题目内容
7.离子键的强弱主要决定于离子半径和离子电荷数,一般规律是:离子半径小,离子所带电荷值大,则离子键越强.①K2O ②MgO ③CaO三种物质离子键由强到弱的顺序是( )| A. | K2O、MgO、CaO | B. | MgO、CaO、K2O | C. | MgO、K2O、CaO | D. | CaO、K2O、MgO |
分析 根据离子半径Mg2+<Ca2+<K+以及离子电荷数K+<Mg2+=Ca2+结合影响离子键强弱的因素解答.
解答 解:离子半径Mg2+<Ca2+<K+,
离子电荷数K+<Mg2+=Ca2+,
离子半径越小,电荷值越大,则离子键越强,
则离子键由强到弱的顺序是MgO>CaO>K2O,
故选B.
点评 本题考查离子键的比较,题目难度不大,注意把握影响离子键强弱的因素,把握离子半径大小的比较方法.

练习册系列答案
相关题目
17.下列变化过程,属于放热反应的是( )
①液态水变成水蒸气
②酸碱中和反应
③金属钠与水的反应
④氧化钙与二氧化碳的反应
⑤H2在Cl2中燃烧
⑥熟石灰与氯化铵的反应.
①液态水变成水蒸气
②酸碱中和反应
③金属钠与水的反应
④氧化钙与二氧化碳的反应
⑤H2在Cl2中燃烧
⑥熟石灰与氯化铵的反应.
| A. | ②③④⑤ | B. | ②③④ | C. | ②⑤ | D. | ①③⑤ |
18.下列叙述不正确的是( )
| A. | Ag+和Cl-在水溶液中的反应,其活化能为零 | |
| B. | 化学反应的反应热只与反应体系的始态和终点状态有关,而与反应的途径无关 | |
| C. | 放热反应一定能自发进行,而吸热反应一定不能自发进行 | |
| D. | 熵增且放热的反应一定自发进行,但实际可能因速率很小而不一定发生 |
2.下表为元素周期表的一部分,请回答有关问题:
(1)⑤和⑧的元素符号和名称是硅 Si和氩Ar;
(2)表中最活泼的金属是Na,非金属最强的元素是F;(填写元素符号)
(3)表中能形成两性氢氧化物的元素是Al;
(4)⑨单质与水反应的化学方程式为2Na+2H2O=2NaOH+H2↑.
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | ① | ② | ||||||
| 3 | ⑨ | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(2)表中最活泼的金属是Na,非金属最强的元素是F;(填写元素符号)
(3)表中能形成两性氢氧化物的元素是Al;
(4)⑨单质与水反应的化学方程式为2Na+2H2O=2NaOH+H2↑.
12.下列有机物的命名正确的是( )
| A. | 3,4,4-三甲基己烷 | B. | 2,2-二甲基戊烷 | ||
| C. | 2-甲基-3-戊炔 | D. | 2-甲基-4-乙基戊烷 |
17.下列说法不正确的是( )
| A. | 含有羟基的化合物不一定属于醇类 | |
| B. | 代表醇类的官能团是与链烃基相连的羟基 | |
| C. | 酚类和醇类具有相同的官能团 | |
| D. | 分子内有苯环和羟基的化合物一定是酚类 |
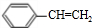 +Br2→
+Br2→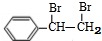 ;在一定条件下,由A聚合得到的高分子化合物的结构简式为
;在一定条件下,由A聚合得到的高分子化合物的结构简式为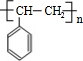 .
.