题目内容
19.(1)等质量的CH4、C3H8、C2H4、C2H2四种烃完全燃烧,消耗氧气最多的是CH4;(2)两种气态烃混和物0.3moL完全燃烧生成0.48moL CO2和10.8gH2O,则混和烃中一定存在CH4;
(3)0.1mol某烃在足量氧气中完全燃烧,生成CO2和H2O各0.6mol,若该烃能与溴水反应褪色,且其核磁共振氢谱中只有一个峰,该烃的结构简式(CH3)2C=C(CH3)2;
(4)某链状烯烃A 的分子式为C6H10,它的分子结构中无支链.它与Br21:1加成可以得到三种产物,则A 的结构简式为CH2=CHCH=CHCH2CH3;
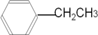
(5)含苯环的某烃A,其相对分子质量为104,碳的质量分数为92.3%.A与溴的四氯化碳溶液反应的化学方程式为
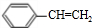 +Br2→
+Br2→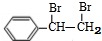 ;在一定条件下,由A聚合得到的高分子化合物的结构简式为
;在一定条件下,由A聚合得到的高分子化合物的结构简式为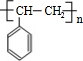 .
.
分析 (1)等质量的烃完全燃烧,H元素质量分数越大耗氧量越大;
(2)n(H2O)=$\frac{10.8g}{18g/mol}$=0.6mol,则混合的平均化学式为C1.6H4,由于是混合物,则肯定含有C原子数小于1.5的烃,即一定含有甲烷,因甲烷中含有4个氢原子,则另一种烃也含有4个氢原子;
(3)根据元素守恒确定烃的分子式,若该烃能与溴水反应褪色,含有不饱和键,再结合其核磁共振氢谱中只有一个峰确定其结构简式;
(4)某链状烯烃A 的分子式为C6H10,它的分子结构中无支链,其不饱和度为$\frac{2×6+2-10}{2}$=2,它与Br21:1加成可以得到三种产物,则A含有2个碳碳双键,且存在C=C-C=C结构;
(5)含苯环的某烃A,其相对分子质量为104,碳的质量分数为92.3%,分子中C原子数目为$\frac{104×92.3%}{12}$=8、H原子数目为$\frac{104-12×8}{1}$=8,则A的结构简式为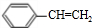 .
.
解答 解:(1)等质量的烃完全燃烧,H元素质量分数越大耗氧量越大,CH4、C3H8、C2H4、C2H2四种中CH4中氢元素质量分数最大,则CH4完全燃烧消耗氧气最多,故答案为:CH4;
(2)n(H2O)=$\frac{10.8g}{18g/mol}$=0.6mol,由原子守恒可知,混合的平均化学式为C1.6H4,由于是混合物,则肯定含有C原子数小于1.5的烃,即一定含有甲烷,因甲烷中含有4个氢原子,则另一种烃也含有4个氢原子,故答案为:CH4;
(3)0.1mol某烃在足量氧气中完全燃烧,生成CO2和H2O各0.6mol,由原子守恒可知,该烃的分子式为:C6H12,若该烃能与溴水反应褪色,含有一个碳碳双键,且其核磁共振氢谱中只有一个峰,该烃的结构简式为:(CH3)2C=C(CH3)2,故答案为:(CH3)2C=C(CH3)2;
(4)某链状烯烃A 的分子式为C6H10,它的分子结构中无支链,其不饱和度为$\frac{2×6+2-10}{2}$=2,它与Br21:1加成可以得到三种产物,则A含有2个碳碳双键,且存在C=C-C=C结构,则该烃的结构简式为:CH2=CHCH=CHCH2CH3,故答案为:CH2=CHCH=CHCH2CH3;
(5)含苯环的某烃A,其相对分子质量为104,碳的质量分数为92.3%,分子中C原子数目为$\frac{104×92.3%}{12}$=8、H原子数目为$\frac{104-12×8}{1}$=8,则A的结构简式为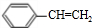 ,A与溴的四氯化碳溶液反应的化学方程式为:
,A与溴的四氯化碳溶液反应的化学方程式为: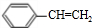 +Br2→
+Br2→ 在一定条件下,由A聚合得到的高分子化合物的结构简式为
在一定条件下,由A聚合得到的高分子化合物的结构简式为 ,
,
故答案为: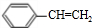 +Br2→
+Br2→ ;
; .
.
点评 本题考查有机物推断、化学方程式计算等,难度不大,(2)中注意平均分子式的应用.

| 实验步骤 | 主要操作过程 | 离子方程式 |
| (1) | ||
| (2) | 过滤,得到不溶物和滤液 | |
| (3) | ||
| (4) | ||
| (5) | 将滤液合并,蒸发浓缩,析出晶体 | |
| (6) | , |
| A. | K2O、MgO、CaO | B. | MgO、CaO、K2O | C. | MgO、K2O、CaO | D. | CaO、K2O、MgO |
| A. | Al3+、Al、Mg、K | B. | S、Cl、Cl-、S2- | C. | Na+、Na、Cl、Cl- | D. | Ca2+、K+、S2-、Cl- |
| A. | 1:4 | B. | 1:5 | C. | 2:5 | D. | 1:7 |
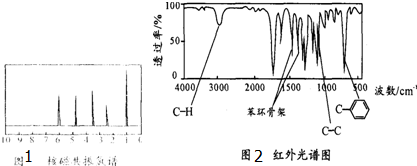
 .
.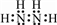 .
. ,N采用sp3杂化方式,粒子空间构型为V型.
,N采用sp3杂化方式,粒子空间构型为V型.