��Ŀ����
15������Ԫ�����ڱ�1��20��Ԫ�ص����ʺ͵ݱ���ɣ��ش��������⣮��1�����ڽ���Ԫ�ص���7�֣���������ǿ��Ԫ����������Ӧ���ɵĻ�����ΪK2O��K2O2
���������ֻ�����Ļ�ѧʽ��
��2���γɻ�������������Ԫ����C
��3�����������У�ԭ�Ӱ뾶�����ǣ�ϡ��������⣩Na��
��4���Ʋ�Si��N����⻯����ȶ��ԣ�NH3ǿ��SiH4���ѧʽ����
��5���縺������Ԫ����F���縺����С��Ԫ����K��
��6��ԭ����p����������Ԫ����N��P��
���� ��1��1��20��Ԫ����Li��Na��K��Ca��Al��Be��Mg��7�ֽ���Ԫ�أ���������ǿ��ΪK���غ���Ԫ�����γ������ء��������صȻ����
��2��̼Ԫ���γ��л���γɵ�����������ࣻ
��3��ͬ�����������ԭ�Ӱ뾶��С��
��4��ͬ����Ԫ�صķǽ���������ԭ���������������ǿ��ͬ�������϶���Ԫ�صķǽ����Լ�����Ԫ�صķǽ�����Խǿ�����⻯��Խ�ȶ���
��5��ͬ���ڴ����ҵ縺��������ͬ������ϵ��µ縺����С��
��6��p��������6�����ӣ����p�����������p�������3�����ӣ�Ϊ��VA��Ԫ�أ�
��� �⣺��1��1��20��Ԫ����Li��Na��K��Ca��Al��Be��Mg��7�ֽ���Ԫ�أ���������ǿ��ΪK��K��O2��������K2O��K2O2�ȣ�
�ʴ�Ϊ��7��K2O��K2O2��
��2��̼Ԫ���γ��л���γɵ�����������࣬�ʴ�Ϊ��C��
��3��ͬ�����������ԭ�Ӱ뾶��С���ʵ��������а뾶����Ԫ����Na���ʴ�Ϊ��Na��
��4������N�ķǽ����Ա�Siǿ�����NH3��SiH4�ȶ����ʴ�Ϊ��NH3��SiH4��
��5��ͬ���ڴ����ҵ縺��������ͬ������ϵ��µ縺����С���ʵ縺������Ԫ����F����С����K���ʴ�Ϊ��F��K��
��6��p��������6�����ӣ����p�����������p�������3�����ӣ�Ϊ��VA��Ԫ�أ�ԭ������С��20�ĵ�VA��Ԫ�طֱ���N��P���ʴ�Ϊ��N��P��
���� ���⿼��Ԫ�������ɺ�Ԫ�����ڱ�����������Ų��ȣ�ע��Ի���֪ʶ���������գ��ѶȲ���

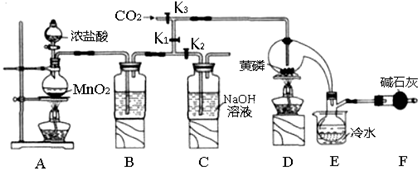
��֪����������Cl2��Ӧ����PCl3�������Cl2��Ӧ����PCl5 PCl3��ˮ��ǿ��ˮ���� �� H3PO3��HC1����O2������P0Cl3��P0Cl3����PCl3��PCl3��POCl3���۷е���±���
| ���� | �۵�/�� | �е�/�� |
| PCl3 | -112 | 75.5 |
| POCl3 | 2 | 105.3 |
��1��Aװ���������������ӷ���ʽΪMnO2+4H++2Cl-$\frac{\underline{\;����\;}}{\;}$Mn2++Cl2��+2H2O��
��2��B����װ�Լ���ŨHSO4��E����ˮ������������PCl3��ֹ��ӷ�F�м�ʯ�ҵ����������ն������������ֹ�����е�ˮ��PCl3��Ӧ
��3��ʵ��ʱ�����װ�������Ժ��ȴ�K3ͨ������CO2����Ѹ�ټ�����ף�ͨ����CO2���������ž�װ���еĿ�������ֹ������ȼ��
��4���ֲ�Ʒ�г�����POCl3��PCl5�ȣ���������ȳ�ȥPCl5��ͨ��������ʵ��������ƣ������ɵõ��ϴ�����PCl3��
��5��ͨ�����淽���ɲⶨ��Ʒ��PCl3����������
��Ѹ�ٳ�ȡ1.00g��Ʒ����ˮ��Ӧ�����250mL��Һ��
��ȡ������Һ25.00mL�������м���10.00mL 0.1000mol•L-1��ˮ����ַ�Ӧ��
�����������Һ�м��뼸�ε�����Һ����0.1000mol•L-1��Na2S2O3����Һ�ζ�
���ظ��ڡ��۲�����ƽ������Na2S2O3����Һ8.40ml
��֪��H3PO3+H2O+I2�TH3PO4+2HI��I2+2Na2S2O3�T2NaI+Na2S4O6������ⶨ������û��������Ӧ�������������ݣ��ò�Ʒ��PC13����������Ϊ79.75%��
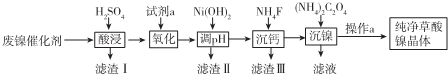
��֪������ؽ������������������������pH���±���
| �������� | Fe3+ | Fe2+ | Al3+ | Ni2+ |
| ��ʼ������pH | 1.1 | 5.8 | 3.0 | 6.8 |
| ��ȫ������pH | 3.2 | 8.8 | 5.0 | 9.5 |
�۵�ij����ģ��߶�С��1.0��10-5mol��L-1ʱ����Ϊ��ȫ������
��1����д��һ�������������ʵĴ�ʩ�ѷ�������������ʵ����ȡ��ʵ���������Ũ�ȡ�����ȣ�
��2���Լ�a��һ����ɫ��������д����������ʱ��Ӧ�����ӷ���ʽ2Fe2++H2O2+2H+=2Fe3++2H2O��
��3��pH�ĵ��ط�ΧΪ5.0��6.8�����û�ѧ��Ӧԭ�������֪ʶ��������������ɣ�
��4��д����������ʱ��Ӧ�����ӷ���ʽNi2++C2O42-+2H2O=NiC2O4•2H2O��֤��Ni2+�Ѿ�������ȫ��ʵ�鲽�輰������ȡ�ϲ���Һ�������μӣ�NH4��2C2O4��Һ���������ɣ���Ca2+������ȫʱ����Һ��c��F-����$\sqrt{\frac{1.46��10{\;}^{-10}}{1{0}^{-5}}}$ mol/L��д������ʽ���ɣ���
��5������a�������ǹ��ˡ�ϴ�ӡ����
| A�� | K2O��MgO��CaO | B�� | MgO��CaO��K2O | C�� | MgO��K2O��CaO | D�� | CaO��K2O��MgO |
 ��
�� ��
��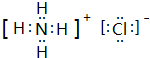 �������Ļ�ѧ������Ϊ���Ӽ������ۼ���
�������Ļ�ѧ������Ϊ���Ӽ������ۼ��� ��
��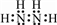 ��
�� ��N����sp3�ӻ���ʽ�����ӿռ乹��ΪV�ͣ�
��N����sp3�ӻ���ʽ�����ӿռ乹��ΪV�ͣ�