题目内容
16.现有A、B、C、D四种短周期元素,它们的核电荷数依次增大.已知A与C,B与D分别是同族元素,且B单质的氧化性比D单质的氧化性强,且B、D两元素的质子数之和是A、C两元素的质子数之和的两倍.其中有一种元素在自然界中含量最丰富.请写出:(1)A元素的名称氢,B元素的符号O.
(2)C元素的单质与A2B反应的离子方程式2Na+2H2O=2Na++2OH-+H2↑.
(3)C元素跟D元素形成的化合物的化学式Na2S.
(4)写出一种均含有四种元素的化合物与碱相互反应的离子方程式HCO3-+OH-═H2O+CO32-.
分析 A、B、C、D四种短周期元素,它们的核电荷数依次增大.其中有一种元素在自然界中含量最丰富,则该元素为O元素,由于A与C,B与D分别是同族元素,B、D两元素的质子数之和是A、C两元素的质子数之和的两倍,可推知B为O元素、D为S元素,A、C元素质子数之和为12,则A为H元素、C为Na元素,据此解答.
解答 解:A、B、C、D四种短周期元素,它们的核电荷数依次增大.其中有一种元素在自然界中含量最丰富,则该元素为O元素,由于A与C,B与D分别是同族元素,B、D两元素的质子数之和是A、C两元素的质子数之和的两倍,可推知B为O元素、D为S元素,A、C元素质子数之和为12,则A为H元素、C为Na元素.
(1)A为氢元素,B为O元素,故答案为:氢;O;
(2)C元素的单质为Na,A2B为水,金属钠与水反应生成氢氧化钠和氢气,反应的离子方程式为:2Na+2H2O=2Na++2OH-+H2↑,故答案为:2Na+2H2O=2Na++2OH-+H2↑;
(3)C元素跟D元素形成的化合物的化学式为Na2S,故答案为:Na2S;
(4)一种均含有四种元素的化合物为碳酸氢钠,碳酸氢钠与碱溶液反应生成碳酸钠和水,反应的离子方程式为:HCO3-+OH-═H2O+CO32-,故答案为:HCO3-+OH-═H2O+CO32-.
点评 本题考查位置结构与性质关系应用,题目难度中等,推断各元素为解答关键,侧重考查学生分析推理能力,需要注意熟练掌握原子结构与元素周期表.

练习册系列答案
相关题目
7.离子键的强弱主要决定于离子半径和离子电荷数,一般规律是:离子半径小,离子所带电荷值大,则离子键越强.①K2O ②MgO ③CaO三种物质离子键由强到弱的顺序是( )
| A. | K2O、MgO、CaO | B. | MgO、CaO、K2O | C. | MgO、K2O、CaO | D. | CaO、K2O、MgO |
1.下列物质的变化中,有共价键明显被破坏的是( )
| A. | I2升华 | B. | NaCl颗粒被粉碎 | ||
| C. | 溴蒸汽被木炭吸附 | D. | 从NH4HCO3中闻到了刺激性气味 |
8.下列各组微粒中,半径依次增大的是( )
| A. | Al3+、Al、Mg、K | B. | S、Cl、Cl-、S2- | C. | Na+、Na、Cl、Cl- | D. | Ca2+、K+、S2-、Cl- |
 .
.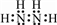 .
. ,N采用sp3杂化方式,粒子空间构型为V型.
,N采用sp3杂化方式,粒子空间构型为V型.