题目内容
【题目】已知A、B、D、E均为中学化学常见单质或化合物,它们之间的关系如图所示[部分产物略去]。下列说法错误的是
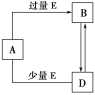
A.A、B、D可能是钠及其化合物B.A、B、D可能是铁及其化合物
C.A、B、D可能是铝及其化合物D.A、B、D不可能是非金属及其化合物
【答案】D
【解析】
A、假设A、B、D含钠及其化合物,A为NaOH,E为CO,NaOH与过量的CO2反应生成NaHCO3,即B为NaHCO3,NaOH与少量的CO2反应生成Na2CO3,即D为Na2CO3,NaHCO3受热分解成Na2CO3,Na2CO3与CO2、H2O反应生成NaHCO3,符合该转化关系,故A说法正确;
B、假设A、B、D可能是铁及其化合物,令A为Fe,E为HNO3,铁与过量的HNO3反应生成Fe(NO3)3,铁与少量的HNO3反应生成Fe(NO3)2,Fe(NO3)3与Fe反应生成Fe(NO3)2,Fe(NO3)2与氧化剂反应生成fFe(NO3)3,符合转化关系,故B说法正确;
C、假设A、B、D为铝及其化合物,令A为AlCl3,E为NaOH,AlCl3与过量的NaOH反应生成NaAlO2,AlCl3与少量的NaOH溶液反应生成Al(OH)3,AlO2-与H+反应生成Al(OH)3,Al(OH)3与NaOH反应生成NaAlO2,符合转化关系,故C说法正确;
D、假设A、B、D为碳及其化合物,令A为C,E为O2,C与足量的O2反应生成CO2,与少量的O2反应生成CO,CO2与C反应生成CO,CO与O2反应生成CO2,符合转化关系,因此A、B、D可能是非金属及其化合物,故D说法错误;
答案为D。

【题目】X、Y、Z、W为短周期元素,若W原子的最外层电子数是其内层电子的![]() ,如图所示,下列说法不正确的是
,如图所示,下列说法不正确的是
X | Y | |
Z | W |
A.X元素的氢化物分子间可以形成氢键
B.Y元素的两种同素异形体常温下都是气体
C.阴离子半径从大到小的顺序为X>Y>Z>W
D.最高价氧化物对应的水化物的酸性:W>Z
【题目】请参照元素①-⑧在表中的位置,根据判断出的元素回答问题:
① | |||||||
② | ③ | ④ | |||||
⑤ | ⑥ | ⑦ | ⑧ |
(1)⑧原子的最外层电子的轨道表达式为___________________,关于它的最外层p亚层电子的说法错误的是_________。(填序号)
a. 能量相同 b.电子云形状相同
c. 自旋方向相同 d. 电子云伸展方向相同
(2)③和①组成的四核分子的化学式为___________,空间构型为_____________,属于_____分子(填“极性”或“非极性”)。
(3)比较④、⑤元素常见离子的半径大小(用化学式表示)______>_____;②、③ 两元素非金属性较强的是 ______(写元素符号),写出证明该结论的一个事实:___________________________ 。
(4)④、⑤元素形成的四原子化合物的电子式为 ___________ ;已知⑥元素的氧化物的熔点为2054℃,且以它为原料,可以通过电解的方法得到铝,据此推断⑥元素的氧化物为_________晶体(填“分子晶体”或“离子晶体”或“原子晶体”或“金属晶体”)。⑥元素的氧化物熔点______⑥元素的氯化物熔点(填“大于”“小于”“等于”),请解释其原因______________________________。