题目内容
【题目】黄铜灰渣(含有Cu、Zn、CuO、ZnO 及少量的FeO、Fe2O3) 生产氯化铜晶体的流程如下:

(1)反应I中所加Zn 粉不能过量的原因是_____________。
(2)滤液I中含有的主要金属阳离子是_____________。
(3) 写出反应II 的化学方程式_____________。
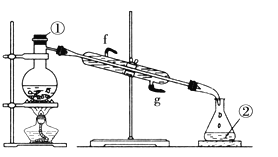
(4)“系列操作”包括蒸发浓缩、冷却结晶、过滤、______、_____。
(5) 在空气中直接加热CuCl2·xH2O晶体得不到纯的无水CuCl2,原因是_____________。
(6) 298K 时,向c (Cu2+) =0.02mol/L的溶液中加入氢氧化钠来调节溶液的pH,若反应后溶液pH=10,此时Cu2+是否沉淀完全? _____{列式计算,己知:Ksp[Cu(OH)2] =2.2×10-20,c(Cu2+)<1×10-5mol/L 视为沉淀完全}_____。
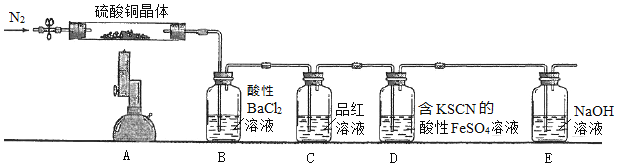
(7) CuCl2·xH2O晶体中x值的测定:称取3.420 g 产品溶解于适量水中,向其中加入含AgNO34.400×10-2mol 的AgNO3溶液(溶液中除Cl- 外,不含其他与Ag+反应的离子),待C1-完全沉淀后,用含Fe3+的溶液作指示剂,用0.2000 mol/L 的KSCN 标准溶液滴定剩余的AgNO3。使剩余的Ag+以AgSCN 白色沉淀的形式析出。
①滴定终点的现象是__________。
②若滴定过程用去上述浓度的KSCN 标准溶液20.00mL,则CuCl2·xH2O中x值为_____。
【答案】 加入过量的Zn会使产品中含有杂质 Zn2+、Fe2+ Cu+H2O2+2HCl=CuCl2+2H2O 洗涤 干燥 Cu2+会水解 是 溶液pH=10,则c(OH-)=10-4mol/L,Ksp [Cu(OH)2]= c(Cu2+) c2(OH-) = c(Cu2+)×(10-4mol/L)2=2.2×10-20,此时c(Cu2+)=2.2×10-12<1×10-5mol/L,故Cu2+沉淀完全 溶液变为红色,且30s不褪色 2
【解析】黄铜灰中加入稀盐酸,稀盐酸可与Zn、CuO、ZnO、FeO、Fe2O3反应,滤渣1为铜,滤液1主要含有Zn2+、Cu2+、Fe2+、H+,加入适量锌粉,锌粉先与Cu2+、H+反应生成铜单质,滤渣2主要为铜,与滤渣1合并为铜。铜在双氧水及过量盐酸反应生成氯化铜,在氯化氢的氛围中蒸发结晶得到氯化铜晶体。(1)反应I中所加Zn不能过量若加入过量的Zn会同时置换出铁,使产品中含有杂质;(2)滤液I中含有的主要金属阳离子是Zn2+、Fe2+;(3)反应II是铜在双氧水和盐酸中反应生成氯化铜和水,反应的化学方程式为Cu+H2O2+2HCl=CuCl2+2H2O;(4)“系列操作”包括蒸发浓缩、冷却结晶、过滤、洗涤、干燥;(5)在空气中直接加热CuCl2·xH2O晶体得不到纯的无水CuCl2,原因是Cu2+会水解产生氢氧化铜和盐酸,加热时盐酸挥发,最后剩下氢氧化铜;(6)溶液pH=10,则c(OH-)=10-4mol/L,Ksp [Cu(OH)2]= c(Cu2+) c2(OH-) = c(Cu2+)×(10-4mol/L)2=2.2×10-20,此时c(Cu2+)=2.2×10-12<1×10-5mol/L,故Cu2+沉淀完全;(7) ①滴定终点时SCN-遇铁离子遇红色,则现象是溶液变为红色,且30s不褪色;②与KSCN反应的银离子的物质的量为0.2000mol/L×0.020L=0.004mol,CuCl2·xH2O晶体n(Cl-)=4.400×10-2mol-0.004mol=0.0400mol,则 ,解得x=2。
,解得x=2。

【题目】二甲醚又称甲醚,简称DME,熔点-141.5℃,沸点-24.9℃,与石油液化气(LPG) 相似,被誉为“21世纪的清洁燃料”。制备原理如下:
I.由天然气催化制备二甲醚:
①2CH4(g)+O2(g)![]() CH3OCH3(g) +H2O(g) △H1=- 283.6 kJ/mol
CH3OCH3(g) +H2O(g) △H1=- 283.6 kJ/mol
II.由合成气制备二甲醚:
②CO(g) +2H2(g)![]() CH3OH(g) △H2=- 90.7 kJ/mol
CH3OH(g) △H2=- 90.7 kJ/mol
③2CH3OH (g)![]() CH3OCH3(g) +H2O(g) △H3
CH3OCH3(g) +H2O(g) △H3
回答下列问题:
(1) 反应③中的相关的化学键键能数据如表:
化学键 | H—H | C—O | H—O(水) | H—O(醇) | C—H |
E/(kJ/mol ) | 436 | 343 | 465 | 453 | 413 |
△H3=_______kJ/mol。

(2) 制备原理I中,在恒温、恒容的密闭容器中合成,将气体按n(CH4): n(O2) =2: 1混合,能正确反映反应①中CH4的体积分数随温度变化的曲线是_______。下列能表明反应①达到化学平衡状态的是________。
a.混合气体的密度不变
b.反应容器中二甲醚的百分含量不变
c.反应物的反应速率与生成物的反应速率之比等于化学计量数之比
d.混合气体的压强不变
(3) 有人模拟制备原理II,在500K时的2L 的密闭容器中充入2mol CO和6mol H2,8min达到平衡,平衡时CO 的转化率为80%,c(CH3OCH3)=0.3mol/L,用H2表示反应②的速率是______;可逆反应③的平衡常数K=_______。若在500K 时,测得容器中n(CH3OH)=n(CH3OCH3),此时反应③v ( 正)______v (逆),说明原因________________。
【题目】25 ℃,两种酸的电离常数如下右表。下列说法正确的是
酸 | Ka1 | Ka2 |
H2SO3 | 1.3×10-2 | 6.3×10-6 |
H2CO3 | 4.2×10-7 | 5.6×10-11 |
A. H2CO3的电离方程式为H2CO3![]() 2H++CO
2H++CO![]()
B. 酸性强弱顺序为H2SO3>H2CO3>HSO>HCO
C. 0.2 mol/L Na2CO3溶液中离子浓度大小顺序为:c(Na+)>c(CO![]() )>c(HCO)>c(OH-)>c(H+)
)>c(HCO)>c(OH-)>c(H+)
D. 足量SO2气体通入NaHCO3溶液中,反应的离子方程式为SO2+HCO==HSO+CO2