题目内容
【题目】二甲醚又称甲醚,简称DME,熔点-141.5℃,沸点-24.9℃,与石油液化气(LPG) 相似,被誉为“21世纪的清洁燃料”。制备原理如下:
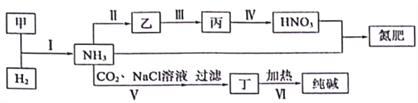
I.由天然气催化制备二甲醚:
①2CH4(g)+O2(g)![]() CH3OCH3(g) +H2O(g) △H1=- 283.6 kJ/mol
CH3OCH3(g) +H2O(g) △H1=- 283.6 kJ/mol
II.由合成气制备二甲醚:
②CO(g) +2H2(g)![]() CH3OH(g) △H2=- 90.7 kJ/mol
CH3OH(g) △H2=- 90.7 kJ/mol
③2CH3OH (g)![]() CH3OCH3(g) +H2O(g) △H3
CH3OCH3(g) +H2O(g) △H3
回答下列问题:
(1) 反应③中的相关的化学键键能数据如表:
化学键 | H—H | C—O | H—O(水) | H—O(醇) | C—H |
E/(kJ/mol ) | 436 | 343 | 465 | 453 | 413 |
△H3=_______kJ/mol。

(2) 制备原理I中,在恒温、恒容的密闭容器中合成,将气体按n(CH4): n(O2) =2: 1混合,能正确反映反应①中CH4的体积分数随温度变化的曲线是_______。下列能表明反应①达到化学平衡状态的是________。
a.混合气体的密度不变
b.反应容器中二甲醚的百分含量不变
c.反应物的反应速率与生成物的反应速率之比等于化学计量数之比
d.混合气体的压强不变
(3) 有人模拟制备原理II,在500K时的2L 的密闭容器中充入2mol CO和6mol H2,8min达到平衡,平衡时CO 的转化率为80%,c(CH3OCH3)=0.3mol/L,用H2表示反应②的速率是______;可逆反应③的平衡常数K=_______。若在500K 时,测得容器中n(CH3OH)=n(CH3OCH3),此时反应③v ( 正)______v (逆),说明原因________________。
【答案】 -24kJ/mol b bd 0.2mol/(L·min) 2.25 > 浓度商Q<2.25,反应正向进行,V(正)>v(逆)
【解析】(1)反应③2CH3OH(g)![]() CH3OCH3(g)+H2O(g) △H3=反应物总键能-生成物总键能=
CH3OCH3(g)+H2O(g) △H3=反应物总键能-生成物总键能=![]() =-24kJ/mol;(2)升温,反应①2CH4(g)+O2(g)
=-24kJ/mol;(2)升温,反应①2CH4(g)+O2(g) ![]() CH3OCH3(g)+H2O(g) △H1=﹣283.6kJ/mol,向逆反应方向移动,能正确反映反应①中CH4的体积分数随温度变化的曲线是b;表明反应①2CH4(g)+O2(g)
CH3OCH3(g)+H2O(g) △H1=﹣283.6kJ/mol,向逆反应方向移动,能正确反映反应①中CH4的体积分数随温度变化的曲线是b;表明反应①2CH4(g)+O2(g) ![]() CH3OCH3(g)+H2O(g)达到化学平衡状态的a.混合气体的密度始终不变,故a错误;b.反应容器中二甲醚的百分含量不变,表明达到平衡,故b正确;c.反应物的反应速率与生成物的反应速率之比始终等于化学计量数之比;故c错误;d.混合气体的压强不变,表明达到平衡,故d正确。答案选bd;
CH3OCH3(g)+H2O(g)达到化学平衡状态的a.混合气体的密度始终不变,故a错误;b.反应容器中二甲醚的百分含量不变,表明达到平衡,故b正确;c.反应物的反应速率与生成物的反应速率之比始终等于化学计量数之比;故c错误;d.混合气体的压强不变,表明达到平衡,故d正确。答案选bd;
(3) CO(g)+2H2(g) ![]() CH3OH(g)
CH3OH(g)
起始量(mol/L) 1 3 0
转化量(mol/L) 0.8 1.6 0.8
平衡量(mol/L) 0.2 1.4 0.8
v(H2)= ![]() =0.2mol/(Lmin);
=0.2mol/(Lmin);
2CH3OH(g) ![]() CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)
起始量(mol/L) 0.8 0 0
转化量(mol/L) 0.6 0.3 0.3
平衡量(mol/L) 0.2 0.3 0.3
k= ![]() = 2.25;
= 2.25;
若在500K时,容器中n(CH3OH)=n(CH3OCH3)时,设c(CH3OH)=x mol/L,则
2CH3OH(g) ![]() CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)
在500K时,容器中(mol/L) x x x
浓度商Q=![]() =1<2.25,反应正向进行,v(正)>v(逆)。
=1<2.25,反应正向进行,v(正)>v(逆)。

【题目】X、Y、Z、W是元素周期表中前36号元素,且原子序数依次增大。其相关信息如下表:
元素编号 | 元素性质或原子结构 |
X | X原子的最外层电子数是其内层电子总数的2倍 |
Y | Y的基态原子价电子排布式为nsnnpn+2 |
Z | 最外层中只有两对成对电子 |
W | 前四周期基态原子中,W元素的未成对电子数最多 |
(1)元素X最高价氧化物分子的空间构型是__________________,是_________(填“极性”或“非极性”)分子。
(2)Y的最简单氢化物的沸点比Z的最简单氢化物的沸点高,原因是____________________________________
(3)基态Z原子中,电子占据的最高电子层符号为_________,该电子层具有的原子轨道数为________________
(4)元素W位于元素周期表的第________族。