题目内容
【题目】实验室用少量的溴水和足量的乙醇制备1,2-二溴乙烷的装置如下图所示:
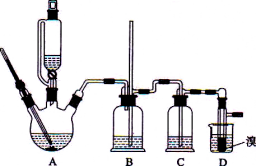
有关数据列表如下:
乙醇 | 1,2-二溴乙烷 | 醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/g · cm-3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | -l30 | 9 | -1l6 |
回答下列问题:
(1)烧瓶A中发生的主要的反应方程式_____________________。
(2)装置B的作用是_____________________。
(3)在装置C中应加入___________(填字母)
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(4)若产物中有少量未反应的Br2,最好用________(填字母)洗涤除去。
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇 e.Na2SO3溶液
(5)若产物中有少量副产物乙醚.可用_______________的方法除去。
(6)反应过程中应用冷水冷却装置D,但又不能过度冷却(如用冰水),其原因是_______________。
(7)判断该制备反应已经结束的最简单方法是_____________________。
【答案】(1)CH3CH2OH![]() CH2 = CH2↑+ H2O(2)平衡压强,作安全瓶,防止倒吸。
CH2 = CH2↑+ H2O(2)平衡压强,作安全瓶,防止倒吸。
(3)c(4)e (5)蒸馏(6)产品熔点低,过度冷却会凝固而堵塞导管。(7)D中溴水完全褪色
【解析】
试题分析:A装置是实验室制取乙烯,B是安全瓶,C是排除干扰装置,D是制取1,2-二溴乙烷装置。
(1)根据上述分析,烧瓶A中发生的主要的反应方程式是CH3CH2OH![]() CH2 = CH2↑+ H2O。
CH2 = CH2↑+ H2O。
(2)根据上述分析,装置B是安全瓶,所以装置B的作用是平衡压强,作安全瓶,防止倒吸。
(3)C是排除干扰装置,浓硫酸具有强氧化性,将乙醇氧化成二氧化碳,自身被还原成二氧化硫,二氧化碳、二氧化硫能和氢氧化钠溶液反应,因此,C中加入的是氢氧化钠溶液,其作用是除去可能产生的酸性气体SO2、CO2,答案选c。
(4)因1,2-二溴乙烷在碱性条件下能发生取代反应,所以除去少量的Br2不用NaOH溶液,而是用与Br2反应的Na2SO3溶液,答案选e。
(5)乙醚与其它有机物溶且沸点相关比较大,采用分馏的方法分离。
(6)溴在常温下,易挥发,乙烯与溴反应时放热,溴更易挥发,冷却可避免溴的大量挥发,但1,2-二溴乙烷的凝固点9℃较低,过度冷却会凝固而堵塞导管口,所以不能过度冷却。
(7)乙烯和溴水发生加成反应生成1,2-二溴乙烷,1,2-二溴乙烷为无色,所以判断反应结束的方法是观察D中溴水完全褪色。