题目内容
【题目】由N、B等元素组成的新型材料有着广泛用途。
(1)B2H6是一种高能燃料,它与Cl2反应生成的BCl3可用于半导体掺杂工艺及高纯硅制造,由第二周期元素组成的与BCl3互为等电子体的阴离子为_________(填离子符号,填一个)。
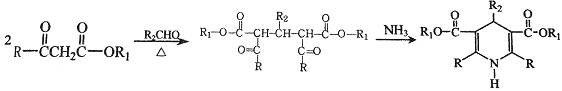
(2)氮硼烷化合物(H2N→BH2)和Ti(BH4)3均为广受关注的新型化学氮化物储氢材料。
①H2N→BH2中N原子的杂化类型为_________;
②Ti(BH4)3由TiCl3和LiBH4反应制得。基态Ti3+的未成对电子数有____个,BH4-的立体构型是_________;写出该制备反应的化学方程式_________;
③氮硼烷可由六元环状化合物(HB=NH)3通过如下所对应制得:
3CH4+2(HB=NH)3+6H2O═3CO2+6H3BNH3与上述化学方程式有关的叙述不正确的是_________;.(填标号)
A.氮硼烷中存在配位键
B.第一电离能:N>O>C>B
C.反应前后碳原子的轨道杂化类型不变
D.CH4、H2O、CO2分子空间构型分别是:正四面体形、V形、直线形
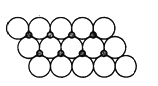
(3)磷化硼(BP)是受到高度关注的耐麿材料;如图1为磷化硼晶胞。
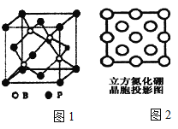
①磷化硼晶体属于________晶体(填晶体类型),________(填是或否)含有配位键。
②晶体中B原子的配位数为_______。
(4)立方氮化硼是一种新型的超硬、耐麿、耐高温的结构材料,其结构和硬度都与金刚石相似,但熔点比金刚石低,原因是________。图2是立方氮化硼晶胞沿z轴的投影图,请在图中圆球上涂“●”和画“×”分别标明B与N的相对位置。
【答案】(1)CO32-或NO3- (2)①sp3 ②1个 正四面体 TiCl3+3LiBH4═Ti(BH4)3+3LiCl ③C
(3)①原子 是 ②4
(4)B—N键键长大于C—C键键长,键能小,所以熔点低 ![]()
【解析】
试题分析:(1)根据等电子体原理,原子数相同,价电子数也相同的粒子互为等电子体,所以由第2周期元素组成的与BCl3互为等电子体的阴离子为CO32-或NO3-;
(2)①H3N→BH3中N原子的价层电子对数为![]() =4,所以N原子的轨道杂化类型为sp3;
=4,所以N原子的轨道杂化类型为sp3;
②基态Ti3+的核外电子排布式为1s22s22p63s23p63d1,其未成对电子数是1,BH4-中B原子的价层电子对数为![]() =4,所以杂化方式为sp3杂化,则BH4-的立体构型为正四面体,Ti(BH4)3由TiCl3和LiBH4反应制得,反应的化学方程式为TiCl3+3LiBH4═Ti(BH4)3+3LiCl;
=4,所以杂化方式为sp3杂化,则BH4-的立体构型为正四面体,Ti(BH4)3由TiCl3和LiBH4反应制得,反应的化学方程式为TiCl3+3LiBH4═Ti(BH4)3+3LiCl;
③A.B一般是形成3个键,(H3BNH3)由六元环状化合物(HB=NH)3通过3CH4+2(HB=NH)3+6H2O→3CO2+6H3BNH3制得,其中1个键是配位键,故A正确;B.同一周期元素中,元素的第一电离能随着原子序数的增大而呈增大趋势,但第IIA族、第VA族元素的第一电离能大于相邻元素,这几种元素都是第二周期元素,它们的族序数分别是:第IIIA族、第IVA族、第VA族、第VIA族,所以它们的第一电离能大小顺序是I1(N)>I1(O)>I1(C)>I1(B),故B正确;
C.由CH4变为CO2,碳原子杂化类型由sp3转化为sp,反应前后碳原子的轨道杂化类型已经改变,故C错误;D.CH4分子中价层电子对=σ 键电子对+中心原子上的孤电子对=4+![]() ×(4-4×1)=4,且不含孤电子对,所以其空间构型是正四面体,H2O中价层电子对个数=2+
×(4-4×1)=4,且不含孤电子对,所以其空间构型是正四面体,H2O中价层电子对个数=2+![]() ×(6-2×1)=4,且含有2个孤电子对,所以H2O的VSEPR模型为四面体,分子空间构型为V型,、CO2分子中价层电子对=σ 键电子对+中心原子上的孤电子对=2+
×(6-2×1)=4,且含有2个孤电子对,所以H2O的VSEPR模型为四面体,分子空间构型为V型,、CO2分子中价层电子对=σ 键电子对+中心原子上的孤电子对=2+![]() ×(4-2×2)=2,所以二氧化碳是直线型结构,故D正确,故答案为C;
×(4-2×2)=2,所以二氧化碳是直线型结构,故D正确,故答案为C;
(3)①在磷化硼晶体中,磷和硼原子之间通过共价键相互作用,结合性质可知其晶体类型为原子晶体,硼最外层有3个电子,但根据晶胞结构可知,每个硼和磷周围都有4个共价键,所以磷原子含有孤电子对,硼原子含有空轨道,它们之间存在配位键;
②根据晶的结构图可知,每个磷原子周围有4个硼原子,所以配位数为4;
(4)立方氮化硼结构和硬度都与金刚石相似,均为原子晶体,B-N键键长大于C-C键,键能小于C-C键,导致立方氮化硼熔点比金刚石低;晶体中B、N原子配位数均为4,涂“●”和画“×”分别标明B与N的相对位置为: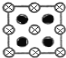 。
。

 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案【题目】下表为元素周期表的一部分用元素符号或化学式回答下列问题。
主族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ⑥ | ① | ⑦ | ④ | ||||
3 | ③ | ⑤ | ⑧ | ⑩ | ||||
4 | ② | ⑨ |
(1)写出⑥与⑧元素组成的分子的电子式:_______。
(2)①的气态氢化物与其最高价氧化物水化物反应的方程式为 , 第三周期中除⑩元素以外离子半径最小的是 (填离子符号)。
(3)②③⑤几种元素最高价氧化物对应的水化物碱性最强的是 (填化学式),元素⑦的氢化物的结构式为 ; 该氢化物和元素④单质反应的化学方程式为 。
(4)元素⑧的单质与②⑨形成的化合物的溶液反应的离子方程式为 。在反应后的溶液中加入有机溶剂苯,震荡后静置的实验现象为 。
(5)与②同主族,第三周期的元素单质在⑦的单质中燃烧生成的化合物的电子式 ;④⑧⑨元素的离子的还原性由强到弱顺序为 (用离子符号)。