题目内容
在200mL氯化镁和氯化铝的混合液中,Mg2+的物质的量浓度为0.2mol/L,Cl-的物质的量浓度为1.3mol/L.要使Mg2+全部转化为沉淀分离出来,至少需要加入4mol/L NaOH溶液的体积为?
考点:化学方程式的有关计算
专题:计算题
分析:根据电荷守恒可知:2n(Mg2+)+3n(Al3+)=n(Cl-),据此计算n(Al3+).欲使Mg2+全部沉淀分离出来,可发生Mg2++2OH-=Mg(OH)2↓,Al3++4OH-=AlO2-+2H2O,Al3+应恰好转化为AlO2-,反应后溶液为NaCl、NaAlO2的混合液,利用Na、Cl、Al原子守恒,有n(NaOH)=n(NaCl)+(NaAlO2)=n(Cl-)+n(Al3+),进而计算需要氢氧化钠溶液体积.
解答:
解:溶液中存在2n(Mg2+)+3n(Al3+)=n(Cl-)=0.2L×1.3mol/L=0.26mol,
因n(Mg2+)=0.2mol/L×0.2L=0.04mol,可知n(Al3+)=
×(0.26mol-0.04mol×2)=0.06mol,
欲使Mg2+全部沉淀分离出来,可发生Mg2++2OH-=Mg(OH)2↓,Al3++4OH-=AlO2-+2H2O,Al3+应恰好转化为AlO2-,反应后溶液为NaCl、NaAlO2的混合液,利用Na、Cl、Al原子守恒,有n(NaOH)=n(NaCl)+(NaAlO2)=n(Cl-)+n(Al3+)=0.26mol+0.06mol=0.32mol,故至少需要加入4mol/L NaOH溶液的体积为
=0.08L=80mL,
答:至少需要加入4mol/L NaOH溶液80mL.
因n(Mg2+)=0.2mol/L×0.2L=0.04mol,可知n(Al3+)=
| 1 |
| 3 |
欲使Mg2+全部沉淀分离出来,可发生Mg2++2OH-=Mg(OH)2↓,Al3++4OH-=AlO2-+2H2O,Al3+应恰好转化为AlO2-,反应后溶液为NaCl、NaAlO2的混合液,利用Na、Cl、Al原子守恒,有n(NaOH)=n(NaCl)+(NaAlO2)=n(Cl-)+n(Al3+)=0.26mol+0.06mol=0.32mol,故至少需要加入4mol/L NaOH溶液的体积为
| 0.32mol |
| 4mol/L |
答:至少需要加入4mol/L NaOH溶液80mL.
点评:本题考查化学方程式有关计算,利用守恒思想简化解题,关键在于清楚反应后溶液为NaCl、NaAlO2的混合液.

练习册系列答案
相关题目
科学家用NaNO3和Na2O在一定条件下化合制得由钠离子和阴离子B构成的晶体NaxNO4,测定阴离子B中的各原子的最外层电子都达到了8电子稳定结构.下列说法错误的是( )
| A、x=3 |
| B、N的化合价为+3 |
C、阴离子B的电子式可能为 |
| D、此反应是非氧化还原反应 |
下列有关金属的工业制法中,正确的是( )
| A、制钠:用海水为原料制得精盐,再电解纯净的NaCl溶液 |
| B、制铁:以铁矿石为原料,用焦炭和空气反应生成CO在高温下还原铁矿石中的铁 |
| C、制镁:用海水为原料,经一系列过程制得氧化镁固体,电解熔融的氧化镁得镁 |
| D、制钛:用金属钠置换TiCl4溶液中的钛 |
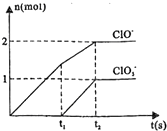 已知NaOH与Cl2反应的氧化产物与温度有关(发生的反应均为放热反应),在V L 4mol/L的NaOH中通入一定量的氯气,生成物中含有Cl-、ClO-、ClO3-三种含氯元素的离子,其中C1O-、ClO3-的物质的量(n)与反应时间(t)的曲线如图所示.
已知NaOH与Cl2反应的氧化产物与温度有关(发生的反应均为放热反应),在V L 4mol/L的NaOH中通入一定量的氯气,生成物中含有Cl-、ClO-、ClO3-三种含氯元素的离子,其中C1O-、ClO3-的物质的量(n)与反应时间(t)的曲线如图所示.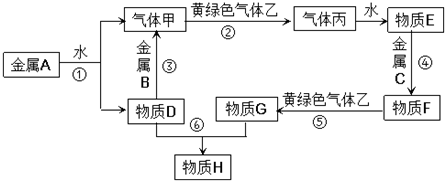
 已知:2KMnO4+16HCl═2KCl+5Cl2↑+2MnCl2+8H2O,如图所示是验证氯气性质的微型实验,a、b、c、d、e是浸有相关溶液的滤纸.向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面.对实验现象的“解释或结论”正确的是( )
已知:2KMnO4+16HCl═2KCl+5Cl2↑+2MnCl2+8H2O,如图所示是验证氯气性质的微型实验,a、b、c、d、e是浸有相关溶液的滤纸.向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面.对实验现象的“解释或结论”正确的是( )