题目内容
下列有关金属的工业制法中,正确的是( )
| A、制钠:用海水为原料制得精盐,再电解纯净的NaCl溶液 |
| B、制铁:以铁矿石为原料,用焦炭和空气反应生成CO在高温下还原铁矿石中的铁 |
| C、制镁:用海水为原料,经一系列过程制得氧化镁固体,电解熔融的氧化镁得镁 |
| D、制钛:用金属钠置换TiCl4溶液中的钛 |
考点:金属冶炼的一般原理
专题:几种重要的金属及其化合物
分析:A.工业制钠是电解熔融NaCl来制取;
B.工业制铁是CO还原铁矿石来制取;
C.工业制镁是电解熔融氯化镁来制取;
D.在一定条件下,钛由四氯化钛(TiCl4)和金属镁反应而制得;
B.工业制铁是CO还原铁矿石来制取;
C.工业制镁是电解熔融氯化镁来制取;
D.在一定条件下,钛由四氯化钛(TiCl4)和金属镁反应而制得;
解答:
解:A.工业制钠是电解熔融NaCl:2NaCl
2Na+Cl2↑,而电解纯净的NaCl溶液:2NaCl+2H2O
2NaOH+H2↑+Cl2↑,得不到钠,故A错误;
B.工业制铁是CO还原铁矿石:3CO+Fe2O3
2Fe+3CO2,故B正确;
C.氧化镁熔点高,工业制镁是电解熔融氯化镁:MgCl2
Mg+Cl2↑,故C错误;
D.钠能与水反应,工业制钛:在氩气的气氛中,用过量的镁在加热条件下与TiCl4反应制得金属钛,TiCl4+2Mg
Ti+2MgCl2,故D错误;
故选B.
| ||
| ||
B.工业制铁是CO还原铁矿石:3CO+Fe2O3
| ||
C.氧化镁熔点高,工业制镁是电解熔融氯化镁:MgCl2
| ||
D.钠能与水反应,工业制钛:在氩气的气氛中,用过量的镁在加热条件下与TiCl4反应制得金属钛,TiCl4+2Mg
| ||
故选B.
点评:本题主要考查了有关金属的工业制法,掌握钠、铁、镁及其化合物的性质是解答的关键,题目难度不大.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
正确掌握化学用语和化学基本概念是学好化学的基础.下列有关表述中正确的一组是( )
| A、16O与18O互为同位素;H216O、D216O、H218O、D218O互为同素异形体 |
| B、SiH4、PH3、HCl的稳定性逐渐增强 |
| C、氧化铁的化学式:FeO |
D、Ca2+的结构示意图为 ,NH4Cl的电子式为 ,NH4Cl的电子式为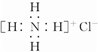 |
下列叙述正确的是( )
| A、液态HCl不导电,所以HCl是非电解质 |
| B、BaSO4难溶于水,但溶于水的部分能够全部电离,所以BaSO4是强电解质 |
| C、CH3COOH溶液的导电能力很弱,所以CH3COOH是弱电解质 |
| D、NH3的水溶液能够导电,所以NH3是电解质 |
设NA为阿伏加德罗常数的值,下列说法中正确的是( )
| A、1.8g NH4+中含有的质子数为NA |
| B、标准状况下,2.24L CO2和SO2混合气中氧原子数为0.1NA |
| C、12g Mg与足量盐酸反应时,失去的电子数为NA |
| D、100mL 1mol?L-1的醋酸溶液中,CH3COO-离子数为0.1NA |
恒温衡容条件,表明反应A(s)+2B(g)?C(g)+D(g)已达平衡的是( )
| A、混合气体的压强不再变化 |
| B、混合气体的密度不再变化 |
| C、生成4mol B的同时消耗2mol C |
| D、气体的总物质的量不再变化 |