题目内容
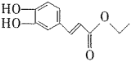
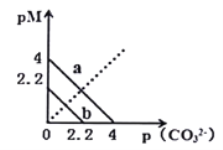
【题目】一定温度下,两种碳酸盐![]() ,(
,(![]() 分别为Ca2+和Ba2+两种离子)的沉淀溶解平衡曲线如图所示。已知:
分别为Ca2+和Ba2+两种离子)的沉淀溶解平衡曲线如图所示。已知:![]() ,
,![]() 。已知
。已知![]() 比
比![]() 溶解度更大(不考虑阴离子的水解)。下列说法正确的是
溶解度更大(不考虑阴离子的水解)。下列说法正确的是
A. 向![]()
![]() 的
的![]() 溶液中加入固体
溶液中加入固体![]() ,当加入
,当加入![]() 固体的质量为
固体的质量为![]() 时,
时,![]() 恰好沉淀完全(离子浓度为
恰好沉淀完全(离子浓度为![]() 时认为沉淀完全;忽略溶液体积变化)
时认为沉淀完全;忽略溶液体积变化)
B. ![]() 的
的![]()
C. 该温度下,向![]() 的饱和溶液中加入
的饱和溶液中加入![]() 溶液,一定能产生沉淀
溶液,一定能产生沉淀
D. 线![]() 表示
表示![]() 的溶解平衡曲线
的溶解平衡曲线
【答案】A
【解析】
A. 碳酸钙的溶解度比碳酸钡更大,则碳酸钙的溶度积大于碳酸钡,曲线a代表碳酸钡的溶解平衡曲线,曲线a知Ksp(BaCO3)=10-4,n(BaCl2)=0.1L×1mol/L=0.1mol;n(Na2CO3)=116.6g/106g/mol=1.1mol,两者反应生成碳酸钡沉淀后,碳酸钠过量,剩余n(CO32-)=1.1mol-0.1mol=1mol,c(CO32-)=1mol/0.1L=10mol/L,此时c(Ba2+)= Ksp(BaCO3)/c(CO32-)(剩)=10-4/10=10-5mol/L,钡离子恰好沉淀完全,A正确;
B. 由曲线b可知,当pM=0时,p(CO32-)=2.2,Ksp(CaCO3)=c(Ca2+)c(CO32-)=1×10-2.2=10-2.2,B错误;
C. 在CaCO3中存在溶解平衡:CaCO3(s)![]() Ca2+(aq)+ CO32-(aq),加入碳酸钠溶液,溶液体积变大,c(Ca2+)减小,c(CO32-)增大,c(Ca2+)×c(CO32-)不一定大于Ksp(CaCO3),不一定产生沉淀,C错误;
Ca2+(aq)+ CO32-(aq),加入碳酸钠溶液,溶液体积变大,c(Ca2+)减小,c(CO32-)增大,c(Ca2+)×c(CO32-)不一定大于Ksp(CaCO3),不一定产生沉淀,C错误;
D. 碳酸钙比碳酸钡溶解度更大,则碳酸钙的溶度积大于碳酸钡;由图可知,曲线a的溶度积小于曲线 b的溶度积,曲线b表示碳酸钙溶解平衡曲线,D错误;
综上所述,本题选A。

 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
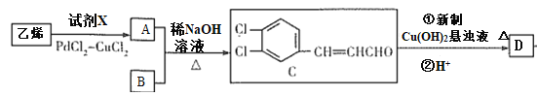
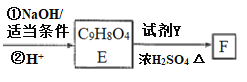
小学同步三练核心密卷系列答案【题目】电子工业上使用![]() 溶液蚀刻铜箔制造印刷电路板。在该制备工艺中,为了实现资源再生,减少污染,某兴趣小组提出废液处理和资源回收的过程如下:
溶液蚀刻铜箔制造印刷电路板。在该制备工艺中,为了实现资源再生,减少污染,某兴趣小组提出废液处理和资源回收的过程如下:
Ⅰ.向废液中投入过量铁屑,充分反应后分离出固体和滤液;
Ⅱ.向滤液中加入一定量石灰水,调节溶液![]() ,同时鼓入足量的空气。
,同时鼓入足量的空气。
已知:Ksp[Fe(OH)3]=4×10-38,回答下列问题:
(1)![]() 蚀刻铜箔反应的离子方程式为______;过程Ⅰ加入铁屑的主要作用是______
蚀刻铜箔反应的离子方程式为______;过程Ⅰ加入铁屑的主要作用是______
(2)过程Ⅱ中鼓入足量的空气发生反应的化学方程式为______
(3)过程Ⅱ中调节溶液的![]() 为5,金属离子浓度为______。(列式计算)
为5,金属离子浓度为______。(列式计算)
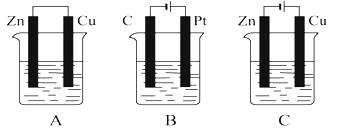
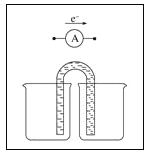
(4)另一兴趣小组将制造印刷电路板![]() 蚀刻铜箔的反应设计成一个原电池。请将方框中实验装置图补充完整,并作相应标注(标出电极材料、电解质溶液)。限选材料:
蚀刻铜箔的反应设计成一个原电池。请将方框中实验装置图补充完整,并作相应标注(标出电极材料、电解质溶液)。限选材料:![]() ,
,![]() ,
,![]() ,
,![]() :铜片,铁片,锌片,石墨和导线。
:铜片,铁片,锌片,石墨和导线。
(5)废旧印刷电路板经粉碎分离能得到非金属粉末和金属粉末,也可回收利用实现资源再生,减少污染。印刷电路板的金属粉末用![]()
![]() 和
和![]()
![]() 的混合溶液处理,溶出印刷电路板金属粉末中的铜。控制其他条件相同时,测得不同温下铜的平均溶解速率(见下表)。
的混合溶液处理,溶出印刷电路板金属粉末中的铜。控制其他条件相同时,测得不同温下铜的平均溶解速率(见下表)。
温度 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
铜平均溶解速率 |
|
|
|
|
|
|
|
①当温度高于![]() 时,铜的平均溶解速率随着反应温度升高而下降,其主要原因是______。
时,铜的平均溶解速率随着反应温度升高而下降,其主要原因是______。
②在提纯后的![]() 溶液中加入一定量的
溶液中加入一定量的![]() 和
和![]() 溶液,加热,生成
溶液,加热,生成![]() 沉淀。制备
沉淀。制备![]() 的离子方程式是______。
的离子方程式是______。