题目内容
【题目】A、B、C、D、E、F六种短周期元素的原子序数依次增大。已知A、C、F位于同一周期,三种元素原子的最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间两两皆能反应,均生成盐和水,D元素原子的最外层电子数比次外层电子数少4个,E元素原子的次外层电子数比最外层电子数多3个。试回答:
(1)写出下列元素的元素符号:
A_____,C_____,D_____,E__________
(2)用电子式表示B、F形成的化合物_____。
(3)A、C两种元素最高价氧化物的水化物之间反应的化学方程式为_____, C、F两种元素最高价氧化物的水化物之间反应的离子方程式为_______________。
【答案】Na Al Si P ![]() Al(OH)3+NaOH=NaAlO2+2H2O Al(OH)3+3H+=Al3++3H2O
Al(OH)3+NaOH=NaAlO2+2H2O Al(OH)3+3H+=Al3++3H2O
【解析】
A、C、F的最高价氧化物的水化物之间两两皆能反应,且这三种元素是处于同一周期的短周期元素,且原子序数依次增大,则C为Al,A为Na,B为Mg。A、C、F原子的最外层共有11个电子,则F为Cl。D元素原子的最外层电子数比次外层电子数少4个,且D为短周期元素,则D的核外电子排布为2、8、4,所以D为Si。E元素原子的次外层电子数比最外层电子数多3个,且E为短周期元素,则E的核外电子排布为2、8、5,所以E为P。综上所述,A为Na,B为Mg,C为Al,D为Si,E为P,F为Cl。
(1)经分析,A为Na,B为Mg,C为Al,D为Si,E为P,F为Cl;
(2) B、F形成的化合物为MgCl2,其电子式为![]() ;
;
(3) A、C两种元素最高价氧化物的水化物分别为NaOH、Al(OH)3,它们之间的化学反应方程式为:Al(OH)3+NaOH=NaAlO2+2H2O;C、F两种元素最高价氧化物的水化物分别为Al(OH)3、HClO4,它们之间的离子反应方程式为:Al(OH)3+3H+=Al3++3H2O。

 黄冈天天练口算题卡系列答案
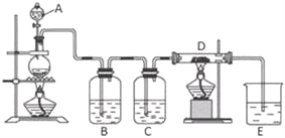
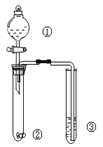
黄冈天天练口算题卡系列答案【题目】利用右图所示装置进行下列实验,能得出相应实验结论的是
选项 | ① | ② | ③ | 实验结论 |
|
A | 稀硫酸 | Na2SO3 | Na2SiO3溶 | 非金属性:S>Si | |
B | 浓硫酸 | 蔗糖 | 溴水 | 浓硫酸具有脱水性、氧化性 | |
C | 稀盐酸 | Na2SO3 | Ba(NO3)2溶液 | SO2与可溶性钡盐均可生成白色沉淀 | |
D | 浓硝酸 | Na2CO3 | Na2SiO3溶液 | 酸性:硝酸>碳酸>硅酸 |
A. A B. B C. C D. D