题目内容
5.能增加反应物分子的活化分子的百分数,同时可以改变化学平衡常数的是( )| A. | 升高温度 | B. | 使用催化剂 | C. | 增大压强 | D. | 增加浓度 |
分析 温度、催化剂改变活化分子百分数,其中催化剂不能使平衡移动,以此解答该题.
解答 解:温度、催化剂,均可提高反应物中的活化分子百分数;而压强和浓度只改变活化分子的浓度,不改变百分数,其中催化剂不改变平衡状态,平衡不移动,只有A符合.
故选A.
点评 本题考查影响反应速率的因素,注意活化分子数目与百分数的差别,明确温度、浓度、压强对反应速率的影响即可解答,注意催化剂不改变平衡状态,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
15.下列化合物中含有离子键的是( )
| A. | CO2 | B. | NaCl | C. | CH4 | D. | H3PO4 |
16.含有元素硒(Se)的保健品已开始进入市场.已知它与氧同族,与钾同周期.则下列关于硒的叙述中,正确的是( )
| A. | 非金属性比硫强 | B. | 最高价氧化物的化学式是SeO2 | ||
| C. | 酸性:H2SeO4>H2SO4 | D. | 气态氢化物的化学式为H2Se |
13.某固体KOH样品含H2O 7.55%、含K2CO3 4.32%,将a g此样品与bmL 1mol/L盐酸反应完全,再用c mol/L KOH溶液25.12mL恰好使剩余盐酸中和.所得的溶液蒸干后,固体的质量为( )
| A. | 0.8a g | B. | 0.0745b g | C. | 0.0376c g | D. | 无法计算 |
20.常温下、用水稀释0.1mol/L氨水时,溶液中随着水量的增加而减小的是( )
| A. | $\frac{c(N{H}_{3}•{H}_{2}O)}{c(O{H}^{-})}$ | B. | $\frac{c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$ | C. | c(H+)和c(OH-)的乘积 | D. | OH-的物质的量 |
14.如图Ⅰ是NO2(g)+CO(g)═CO2(g)+NO(g) 反应过程中能量示意图.一定条件下,在固定容积的密闭容器中该反应达到平衡状态,当改变其中一个条件X,Y随X的变化关系曲线如图Ⅱ.下列有关说法正确的是( )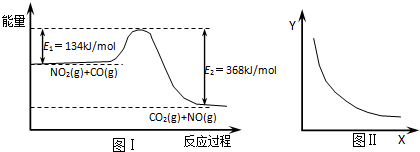

| A. | 该反应的焓变△H=234kJ/mol | |
| B. | 若X表示CO的起始浓度,则Y表示的可能是NO2的转化率 | |
| C. | 若X表示反应时间,则Y表示的可能是混合气体的密度 | |
| D. | 若X表示温度,则Y表示的可能是CO2的物质的量浓度 |
15.下列有关反应限度的叙述正确的是( )
| A. | 大多数化学反应在一定条件下都有一定的限度 | |
| B. | 化学反应在一定条件下达到限度时,正、逆反应速率都等于零 | |
| C. | 当某反应体系中气体压强不在改变时,该反应一定达到了反应限度 | |
| D. | 当某反应在一定条件下达到反应限度时,反应物和生成物的浓度一定相等 |
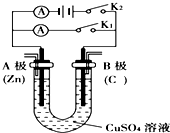 请按要求回答下列问题.
请按要求回答下列问题.