题目内容
3.某无色溶液含有相同浓度的下列离子中的4种离子:K+、Na+、Al3+、Fe3+、Mg2+、Cl-、CO${\;}_{3}^{2-}$、SO42-( )
①取少量溶液于试管中,滴加 BaCl2溶液,有白色沉淀产生,往沉淀中加盐酸,无明显现象
②用干净的铂丝蘸取少量原溶液进行焰色反应,发现火焰颜色为黄色.
| A. | 有现象②可知有 Na+,没有 K+ | |
| B. | 不能确定溶液中有无 Al3+ | |
| C. | 溶液中一定存在 SO${\;}_{4}^{2-}$、Na+、K+ | |
| D. | 溶液中如果存在Cl-则肯定存在 Mg2+ |
分析 根据无色澄清溶液,可得原溶液没有相互反应的离子;根据实验①的现象,判断存在的离子,排除原溶液中与该离子反应的离子;根据实验②的现象,判断存在的离子,排除原溶液中与该离子反应的离子.
解答 解:根据无色澄清溶液,一定没有棕黄色Fe3+,根据①的信息,说明溶液中含有 SO42-,一定没有CO${\;}_{3}^{2-}$;根据②的信息火焰颜色为黄色,说明一定含有钠离子.
A.现象②只能说明含含有 Na+,不能确定 K+,故A错误;
B.不能确定溶液中有无 Al3+,故B正确;
C.不能确定 K+,故C错误;
D.如果存在Cl-,不能确定Mg2+,故D错误.
故选B.
点评 本题考查物质的检验和鉴别,为高频考点,侧重于学生的分析能力和实验能力的考查,可以依据物质的性质进行,注意离子的特征离子反应和现象是关键,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
13.下列各组离子中,相互间不能发生复分解反应的是( )
| A. | Mg2+、NH4+、SO42-、Cl- | B. | Cu2+、Na+、HCO3-、OH- | ||
| C. | K+、Ca2+、NO3-、CO32- | D. | Ag+、Fe3+、Cl-、NO3- |
14.下面是某学生利用数据分析的情况,其中不正确的是( )
| A. | 根据气体的相对分子质量,可以比较相同状况下气体密度的大小 | |
| B. | 根据甲烷和乙烷的熔点,可以比较二者晶体中的分子间作用力的大小 | |
| C. | 比较同周期金属元素原子半径的大小,可以推断元素的金属性强弱 | |
| D. | 根据液体密度的大小,可以判断液体的挥发性的强弱 |
18.RO3n-中共有x个电子,R原子的质量数为A,则a克RO3n-中含有质子的物质的量为( )
| A. | $\frac{a}{A+48}$(x-n)mol | B. | $\frac{a}{A+48}$(x-24-n)mol | C. | $\frac{a}{A+48}$(x+n)mol | D. | (x-n)mol |
8.对于可逆反应2SO2+O$\frac{\underline{\;催化剂\;}}{△}$2SO3,在混合气体中充入一定量18O2,足够长的时间后,18O原子( )
| A. | 只存在于O2中 | B. | 只存在于SO3和O2中 | ||
| C. | 只存在于SO2和O2中 | D. | 存在于SO2、SO3和O2中 |
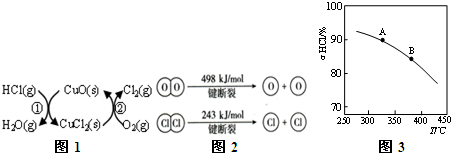
 ,反应A的热化学方程式是4HCl(g)+O2(g)?2Cl2(g)+2H2O(g)△H=-115.6 KJ/mol.
,反应A的热化学方程式是4HCl(g)+O2(g)?2Cl2(g)+2H2O(g)△H=-115.6 KJ/mol.