题目内容
(8分)用氯化铝溶液与氢氧化钠溶液反应时:
(1)当Al3+的物质的量与OH-的物质的量之比为 时,Al(OH)3沉淀量最多;
(2)当Al3+的物质的量与OH-的物质的量之比 时,Al(OH)3全部溶解;
(3)当Al3+的物质的量与OH-的物质的量之比 或 时,Al(OH)3沉淀量为最多沉淀量的一半。
(1)1/3 (2) 1/4 (3) 2/3或2/7
解析试题分析:(1)Al3++3OH-=Al(OH)3↓;Al3++4OH-=AlO2-+ 2H2O。可见当n(OH-) =3n(Al3+),所有的Al3+恰好完全形成沉淀,达到最大值,当n(OH-) =4n(Al3+),形成的沉淀恰好完全溶解,沉淀达到最小值。若3<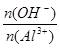 <4,时,沉淀部分溶解,在最大值和最小值之间。若形成的沉淀为最大值的一半,根据反应方程式Al3++3OH-=Al(OH)3↓可知
<4,时,沉淀部分溶解,在最大值和最小值之间。若形成的沉淀为最大值的一半,根据反应方程式Al3++3OH-=Al(OH)3↓可知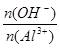 =
=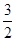 ;当
;当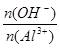 =
=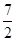 ;形成的沉淀又一半溶解。(1)当Al3+的物质的量与OH-的物质的量之比为1/3时,Al(OH)3沉淀量最多;(2)当Al3+的物质的量与OH-的物质的量之比1/4时,Al(OH)3全部溶解;(3)当Al3+的物质的量与OH-的物质的量之比2/3或2/7时,Al(OH)3沉淀量为最多沉淀量的一半。
;形成的沉淀又一半溶解。(1)当Al3+的物质的量与OH-的物质的量之比为1/3时,Al(OH)3沉淀量最多;(2)当Al3+的物质的量与OH-的物质的量之比1/4时,Al(OH)3全部溶解;(3)当Al3+的物质的量与OH-的物质的量之比2/3或2/7时,Al(OH)3沉淀量为最多沉淀量的一半。
考点:考查氯化铝溶液与氢氧化钠溶液反应时沉淀的物质的量与二者的物质的量的关系的知识。

 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案将1.12g铁粉加入25mL2mol/L的FeCl3溶液中,充分反应后,其结果是( )
| A.铁恰好将Fe3+全部还原 |
| B.往反应后溶液中滴入KSCN溶液,不显红色 |
| C.溶液变为浅绿色 |
| D.Fe2+和Fe3+物质的量之比为6:1 |
金属钠着火时,可用来灭火的是
| A.二氧化碳 | B.水 | C.煤油 | D.沙土 |
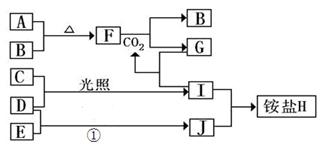
NaCl是一种化工原料,可以制备一系列物质(如图所示)。下列说法正确的是( )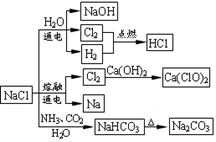
| A.石灰乳与Cl2的反应中Cl2既是氧化剂,又是还原剂 |
| B.25℃,NaHCO3在水中的溶解度比Na2CO3的大 |
| C.常温下干燥Cl2能用钢瓶贮运,所以Cl2与铁不反应 |
| D.图中所示转化反应都是氧化还原反应 |
(12分)某小组进行铝热反应实验,装置如图所示。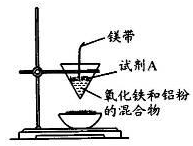
(1)铝热反应原理____(写化学方程式);试剂A为____(写化学式).实验现象____、有黑色固体生成。
(2)对黑色固体物质的组成,小组进行了如下探究
假设I该黑色物质为铁
假设Ⅱ该黑色物质为铁与四氧化三铁的混合物
【设计方案并实验】
| 实 验 步 骤 | 现 象 | 结 论 |
| ①取少量黑色固体于试管中加稀盐酸 | 固体全部溶解,有气泡产生 | 假设I成立,假设Ⅱ不成立 |
| ②滴入几滴0.01mol/LKSCN溶液 | 溶液不变色 |
你认为上述结论是否合理,__ __理由是__ __。
(3)取上述实验所得溶液,滴人适量氯水溶液变红色。此时涉及的离子反应方程式为
__ __、__ __;
利用反应体系中存在的平衡,小组再将溶液均分置于两支试管中并分别编号l、2.进行
如下探究:
| 实验编号 | 实验步骤 |
| 1 | ①滴加饱和FeCl3溶液4滴,充分振荡 |
| ②滴加几滴NaOH溶液 | |
| | ①滴加4滴1mol/LKSCN溶液 |
| ②滴加几滴NaOH溶液 |
主要探究的问题是__ __;
应重点观察的现象是__ __
预计得出的结论是__ __。
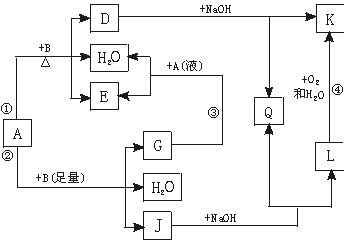
(12分)某研究性学习小组为了测定某品牌合金中铝的含量,现设计了如下实验: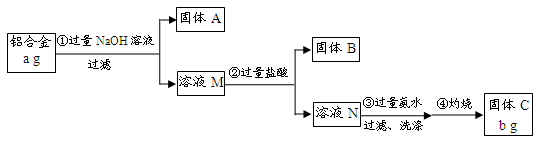
已知:(1)该铝合金的主要成分为铝、镁、铜、硅。
(2)常温下,硅能和NaOH发生反应:Si+2NaOH+H2O===Na2SiO3+2H2↑。
请回答下列问题:
(1)固体A的成分是 ;
(2)生成固体B的离子方程式为 ;
步骤③中生成沉淀的离子方程式为 ;
(3)检验步骤③中沉淀是否洗涤干净的实验操作为
;
(4)该样品中铝的质量分数是 ;(用a、b表示)
(5)下列因操作不当,会使测定结果偏大的是 ;
| A.第①步中加入NaOH溶液不足 | B.第②步中加入盐酸不足时 |
| C.第③步中沉淀未用蒸馏水洗涤 | D.第④步对沉淀灼烧不充分 |
 2Fe(s)+3CO(g) △H=-492.7kJ/mol
2Fe(s)+3CO(g) △H=-492.7kJ/mol