题目内容
将1.12g铁粉加入25mL2mol/L的FeCl3溶液中,充分反应后,其结果是( )
| A.铁恰好将Fe3+全部还原 |
| B.往反应后溶液中滴入KSCN溶液,不显红色 |
| C.溶液变为浅绿色 |
| D.Fe2+和Fe3+物质的量之比为6:1 |
D
解析试题分析:将1.12g铁粉加入到25mL 2mol?L-1的氯化铁溶液中,铁粉的物质的量n=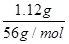 =0.02mol。氯化铁的物质的量n=C×V=2mol?L-1×0.025L=0.05mol,铁粉与氯化铁的离子反应方程式为:Fe+2Fe3+=3Fe2+,根据反应的物质的量之比等于计量数之比知,0.02mol铁粉完全反应需要0.04mol氯化铁。所以氯化铁剩余0.01mol,生成的Fe2+的物质的量为0.06mol。A选项错误。B选项错误,由于溶液中有三节铁离子剩余,故显红色。C选项,由于有三价铁离子剩余,故溶液应为浅绿与红棕的混合色。错误。D选项正确。
=0.02mol。氯化铁的物质的量n=C×V=2mol?L-1×0.025L=0.05mol,铁粉与氯化铁的离子反应方程式为:Fe+2Fe3+=3Fe2+,根据反应的物质的量之比等于计量数之比知,0.02mol铁粉完全反应需要0.04mol氯化铁。所以氯化铁剩余0.01mol,生成的Fe2+的物质的量为0.06mol。A选项错误。B选项错误,由于溶液中有三节铁离子剩余,故显红色。C选项,由于有三价铁离子剩余,故溶液应为浅绿与红棕的混合色。错误。D选项正确。
考点:铁盐和亚铁盐的相互转变

练习册系列答案
相关题目
1 L某混合溶液中,溶质X、Y的浓度都为0.1 mol/L,向混合溶液中滴加某溶液Z(0.1 mol/L氢氧化钠或硫酸溶液)至溶液呈中性,所得沉淀的物质的量如图所示,则X、Y、Z分别是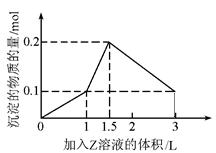
| A.偏铝酸钠、氢氧化钡、硫酸 |
| B.偏铝酸钠、氯化钡、硫酸 |
| C.氯化铝、氯化铁、氢氧化钠 |
| D.氯化铝、氯化镁、氢氧化钠 |
下列各组中的两种物质相互反应时,若改变反应条件(包括温度、反应物浓度、反应物用量比等),化学反应原理不改变的是
| A.Na和O2 | B.NaOH和CO2 | C.NaHCO3与盐酸 | D.MnO2与盐酸 |
将一小块钠投入MgCl2溶液中,下列对有关实验结果的预测正确的是
| A.钠溶解,底部有银白色金属析出,并且有气体产生 |
| B.只有气体产生 |
| C.只有沉淀产生 |
| D.既有沉淀产生,又有气体产生 |
下列关于钠的化合物的叙述中正确的是( )
| A.Na2O和Na2O2都是白色固体 |
| B.Na2CO3能与石灰水反应而NaHCO3不反应 |
| C.Na2CO3受热后稳定性比NaHCO3强 |
| D.Na2O和Na2O2都能与水反应生成O2 |
下列叙述正确的是
| A.将FeCl3溶液加热蒸干得到FeCl3固体 |
| B.向Fe(NO3)2溶液中加少量盐酸,无明显现象 |
| C.向氢氧化镁悬浊液中滴加FeCl3溶液,无明显现象 |
| D.向FeSO4溶液中滴加NaOH溶液,先出现白色沉淀,最终沉淀转化成红褐色 |
金属钠是一种活泼金属,除了具有金属的一般性质外,还具有自己的特性。关于钠的叙述中,正确的是
| A.钠是银白色金属,熔点低,硬度大 |
| B.钠放置在空气中,会迅速被氧化而生成淡黄色的氧化钠 |
| C.加热时,金属钠剧烈燃烧,产生黄色火焰 |
| D.金属钠着火可以用泡沫灭火器或用干燥的沙土灭火 |
4.6g钠投入100g水中,下列叙述错误的是
| A.钠浮在水面,熔化成银色光亮的小球 | B.钠贮存在煤油中 |
| C.所得溶液的质量分数为4.4﹪ | D.该反应中转移0.2mole- |