题目内容
【题目】(1)维生素C又称为抗坏血酸,在人体内有重要的功能。例如,帮助人体将食物中摄取的不易吸收的Fe3+变为易吸收的Fe2+。这说明维生素C具有________(填“氧化性”或“还原性”)。
(2)2Na+O2![]() Na2O2反应中,
Na2O2反应中,
①________被氧化,________是氧化剂,氧化产物是_______,过氧化钠中氧元素的化合价是_______。
②此反应中若转移了2 mol的电子,则需要氧气________ mol。
③用单线桥或双线桥法表示反应中电子转移的方向和数目:______________________。
(3)根据反应①2FeCl3+2KI=2FeCl2+2KCl+I2,②2FeCl2+Cl2=2FeCl3,判断下列物质的氧化性由强到弱的顺序中,正确的是____________。
A.Fe3+>Cl2>I2 B.Cl2>I2>Fe3+
C.I2>Cl2>Fe3+ D.Cl2>Fe3+>I2
【答案】还原性NaO2 Na2O211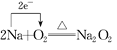
 D
D
【解析】
(1)Fe元素的化合价降低,则维生素C中某元素的化合价升高,说明维生素C具有还原性;
(2)①2Na+O2![]() Na2O2反应中,Na元素的化合价升高,被氧化,Na2O2为氧化产物,O元素的化合价降低,则O2为氧化剂,过氧化钠中氧元素的化合价是-1价;
Na2O2反应中,Na元素的化合价升高,被氧化,Na2O2为氧化产物,O元素的化合价降低,则O2为氧化剂,过氧化钠中氧元素的化合价是-1价;
②由反应可以知道,该反应转移2e-,若转移了2mol的电子,则需要氧气1mol;
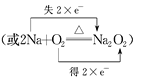
(3) 2Na+O2![]() Na2O2反应中,Na元素的化合价升高,失去的电子数为2,O元素得到的电子数为2,则双线桥法表示反应电子转移的方向和数目为
Na2O2反应中,Na元素的化合价升高,失去的电子数为2,O元素得到的电子数为2,则双线桥法表示反应电子转移的方向和数目为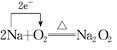
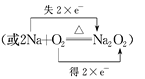 ;
;
(3) ①2FeCl3+2KI=2FeCl2+2KCl+I2,氧化性顺序是Fe3+>I2;②2FeCl2+Cl2=2FeCl3,氧化性顺序是Cl2>Fe3+,所以氧化性顺序是Cl2>Fe3+>I2。故选D。

 能考试全能100分系列答案
能考试全能100分系列答案