题目内容
17.下列说法不正确的是( )| A. | 加热可鉴别碳酸氢钠与碳酸钠 | |
| B. | 焰色反应可鉴别钾盐和钠盐 | |
| C. | 用水可鉴别氢氧化镁和氢氧化铝固体 | |
| D. | KSCN溶液可鉴别Fe3+与Fe2+ |
分析 A.碳酸氢钠不稳定,加热易分解;
B.钾盐和钠盐的焰色反应不同;
C.氢氧化镁和氢氧化铝都不溶于水;
D.Fe3+与KSCN发生显色反应.
解答 解:A.碳酸氢钠不稳定,加热分解生成二氧化碳气体,固体质量减少,可鉴别,故A正确;
B.钾盐和钠盐的焰色反应不同,分别为紫色和黄色,现象不同,可鉴别,故B正确;
C.氢氧化镁和氢氧化铝都不溶于水,氢氧化铝具有两性,可用氢氧化钠溶液鉴别,故C错误;
D.Fe3+与KSCN发生显色反应,溶液呈红色,可鉴别,故D正确.
故选C.
点评 本题考查物质的检验和鉴别,为高频考点,把握物质的性质及性质差异为解答的关键,侧重分析与实验能力的考查,注重实验基础知识的应用,题目难度不大.

练习册系列答案
相关题目
7.分子式为C11H16,含有苯环、-C5H11的有机物的同分异构体有(不考虑立体异构)( )
| A. | 6种 | B. | 8种 | C. | 10种 | D. | 12种 |
8.设NA表示阿伏加德罗常数值,下列说法中正确的是( )
| A. | 1L1 mol•L-1 FeCl3溶液,含有Fe3+的数目为NA个 | |
| B. | 标准状况下,22.4L丙烷中碳碳共价键数目为2NA | |
| C. | 1L0.5 mol•L-1 氨水溶液中含有0.5NA个OH- | |
| D. | 室温下H2O2分解得到16 g O2,转移的电子数为2NA |
5.某小组设计如图装置(盐桥中盛有浸泡了KNO3溶液的琼脂)研究电化学原理.下列叙述正确的是( )

| A. | 银片为正极,发生的反应为:Ag++e-=Ag | |
| B. | 进行实验时,琼脂中K+移向Mg(NO3)2溶液 | |
| C. | 取下盐桥,原电池仍可工作 | |
| D. | 在外电路中,电子从正极流向负极 |
12.某元素的一种同位素AY,其中子数为N,它与1H原子组成HmY分子,则在b g HmY分子中所含质子的物质的量( )
| A. | ($\frac{b}{A}$)(A-N)mol | B. | ($\frac{b}{A}$)(A-N+m)mol | C. | $\frac{b}{A+m}$(A-N)mol | D. | $\frac{b}{A+m}$(A-N+m)mol |
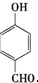 .有人提出,以对甲基苯酚为原料合成PHBA的途径如下:
.有人提出,以对甲基苯酚为原料合成PHBA的途径如下: $→_{①}^{(CH_{3})SO_{4}/OH-}$
$→_{①}^{(CH_{3})SO_{4}/OH-}$ $→_{②}^{Cl_{2}/光照}$C$→_{③}^{NaOH溶液/加热}$D$\stackrel{O_{2}、Cu/加热}{→}$EPHBA
$→_{②}^{Cl_{2}/光照}$C$→_{③}^{NaOH溶液/加热}$D$\stackrel{O_{2}、Cu/加热}{→}$EPHBA
 .
.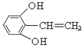 或
或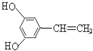 (只写一种).
(只写一种). 可简写为
可简写为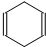 .现有某化合物W的分子结构可表示为:
.现有某化合物W的分子结构可表示为: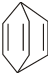 .
.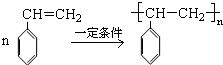 .
.