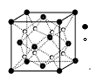
题目内容
短周期元素A、B、C、D、E的原子序数依次增大,A元素阳离子的原子核外没有电子,B是空气中含量最多的元素;C元素原子最外层电子数是其电子层数的三倍;C与D可形成两种常见的离子化合物;工业上常用电解C与E的化合物来制备E单质。
(1)画出D元素的原子结构示意图 。C、D、E的简单离子半径由小到大的顺序 (用离子符号表示)。
(2)写出元素E在周期表中的位置 。
(3)工业上常用A和B的单质合成一种常见气体,检验该气体的常用方法是 。
(4)D2C2与H2O反应的化学方程式是 ,D2C2与CuSO4溶液反应的现象是 。
(5)由元素A、B、C按原子个数比4:2:3形成的化合物,写出其电离方程式: 。
(1) , Al3+<Na+<O2-
(2)第三周期,ⅢA族
(3)用润湿的红色石蕊试纸接近该气体,若试纸变红,证明氨气存在
(4)2Na2O2 + 2H2O =" 4NaOH" + O2↑ 、 产生蓝色沉淀并有气泡放出
(5)NH4NO3=NH4+ + NO3-
解析试题分析:A元素阳离子的原子核外没有电子,所以A是H元素;B是空气中含量最多的元素,所以B是N元素;C元素原子最外层电子数是其电子层数的三倍,则C只能是2层电子,最外层6个电子,则C是O元素;C与D可形成两种常见的离子化合物,则D是Na元素;工业上常用电解C与E的化合物来制备E单质,工业常电解氧化铝来制备铝单质,所以E是Al元素。
(1)Na的原子结构示意图为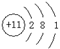
氧离子、钠离子与铝离子的核外电子排布相同,核电荷数越少,半径越大,所以C、D、E的简单离子半径由小到大的顺序是Al3+<Na+<O2-
(2)Al元素位于元素周期表的第三周期,ⅢA族;
(3)A和B的单质合成一种常见气体,该气体是氨气,检验氨气的方法是用润湿的红色石蕊试纸接近该气体,若试纸变红,证明氨气存在;
(4)过氧化钠与H2O反应的化学方程式是2Na2O2 + 2H2O =" 4NaOH" + O2↑;过氧化钠与水反应的产物又与CuSO4溶液反应,所以有气体放出,同时溶液中产生蓝色沉淀;
(5)由元素H、N、O按原子个数比4:2:3形成的化合物是硝酸铵,硝酸铵是强电解质,完全电离,电离方程式为NH4NO3=NH4+ + NO3-
考点:考查原子结构与元素性质的综合应用,原子结构示意图、化学方程式、电离方程式的书写,气体的检验

(15分)下表中列出五种短周期元素X、Y、Z、W、T的信息。
| 元素 | 相关信息 |
| X | 基态原子最外层电子排布为nsnnpn+1 |
| Y | 其原子L层电子数是K层3倍 |
| Z | 其单质能与冷水剧烈反应,生成的阴阳离子电子数相同 |
| W | 其单质在Y2中燃烧,发出明亮的蓝紫色火焰 |
| T | 其最高正价与最低负价的代数和为6 |
回答下列问题:
(1)Y、Z、W三种元素所形成的简单离子半径由小到大的顺序是 (用离子符号表示);T元素的基态原子核外电子排布式为 。
(2)X、Z两元素可形成化合物ZX3,其晶体中化学键类型有 ,晶体类型为 。
(3)T元素的最高价氧化物对应水化物的化学式是 H2Y的沸点比H2W高的原因是 。
(4) Z2 WY3溶液呈 性,其原因是(用离子方程式表示) 。
(5)已知25℃、101 kPa下:
①2Z(s)+
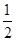 Y2(s)=Z2Y(s) △H1=-414KJ/mol
Y2(s)=Z2Y(s) △H1=-414KJ/mol②2Z(s)+ Y2(s)=Z2Y2(s) △H1=-511KJ/mol
则1mol Z2 Y2(S)与足量Z(s)反应生成Z2 Y(s)的热化学方程式为 。
(13分)短周期元素Q、R、T、W在元素周期表中的位置如右图所示,其中T所处的周期序数与主族序数相等,请回答下列问题: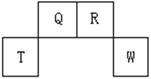
(1)W在周期表中的位置是 , Q、R、T三种元素原子的半径从大到小排列顺序 (用元素符号表示),Q的最高价氧化物的电子式 ,R气态氢化物分子的结构式为 ;
(2)元素的原子得电子能力:Q W(填“强于”或“弱于”);
(3)原子序数比R多8的元素形成的一种常见气态氢化物的沸点 (填“高”或“低”)于R的的常见气态氢化物;
(4)T、Q、R、W的单质中,固态时属于原子晶体的是 (填名称);
(5)现有8种元素的性质、数据如下表所列,它们属于短周期:请指出R元素在下表中的对应编号 ,与T同周期且最高价氧化物的水化物碱性最强的元素在下表中的对应编号 。
| | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径(10-10m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.6 | 0.75 | 0.82 |
| 最高或最低化合价 | | +2 | +1 | +5 | +7 | +1 | +5 | +3 |
| -2 | | | -3 | -1 | | -3 | |
有四种短周期元素,它们的结构、性质等信息如下表所述。
| 元素 | 结构、性质等信息 |
| A | 是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是原子反应堆的导热剂 |
| B | B与A同周期,其最高价氧化物的水化物呈两性 |
| C | 元素的气态氢化物极易溶于水,可用作制冷剂 |
| D | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂 |
请根据表中信息填写:
(1)A原子的核外电子排布式 。
(2)B元素在周期表中的位置 ;
离子半径:B A(填“大于”或“小于”)。
(3)C原子的电子排布图是 ,其原子核外有 个未成对电子,能量最高的电子为 轨道上的电子,其轨道呈 形。
(4)D原子的电子排布式为 ,D-的结构示意图是 。
(5)B的最高价氧化物对应的水化物与A的最高价氧化物对应的水化物反应的化学方程式为 ,与D的氢化物的水化物反应的化学方程式为 。