题目内容
为探究Cl2、漂白粉的制备及有关性质,某兴趣小组设计并进行了以下实验探究。请回答以下问题:
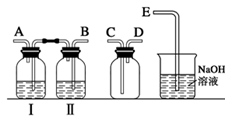
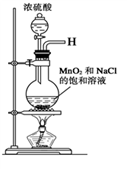
(1)实验室拟用下列装置制备干燥纯净的氯气,请按照气体从左向右流动的方向将仪器进行连接:H→_______、_______→_______、_______→_______;其中广口瓶Ⅱ中的试剂为_______。
(2)写出工业上用氯气和石灰乳制取漂白粉的化学反应方程式_______;
(3)实验室有一瓶密封不严的漂白粉样品,其中肯定存在CaCl2。请设计实验,探究该样品中除CaCl2外还含有的其他固体物质。
①提出合理假设。
假设1:该漂白粉未变质,还含有Ca(ClO)2
假设2:该漂白粉全部变质,还含有______;
假设3:该漂白粉部分变质,还含有Ca(ClO)2和CaCO3。
②设计实验方案,进行实验。请在下表中写出实验步骤、预期现象和结论。
限选用的仪器和药品:试管、滴管、带导管的单孔塞、蒸馏水、自来水、品红溶液、1 mol·L-1 HCl溶液、新制澄清石灰水。(提示:不必检验Ca2+和Cl-。)
(1)实验室拟用下列装置制备干燥纯净的氯气,请按照气体从左向右流动的方向将仪器进行连接:H→_______、_______→_______、_______→_______;其中广口瓶Ⅱ中的试剂为_______。


(2)写出工业上用氯气和石灰乳制取漂白粉的化学反应方程式_______;
(3)实验室有一瓶密封不严的漂白粉样品,其中肯定存在CaCl2。请设计实验,探究该样品中除CaCl2外还含有的其他固体物质。
①提出合理假设。
假设1:该漂白粉未变质,还含有Ca(ClO)2
假设2:该漂白粉全部变质,还含有______;
假设3:该漂白粉部分变质,还含有Ca(ClO)2和CaCO3。
②设计实验方案,进行实验。请在下表中写出实验步骤、预期现象和结论。
限选用的仪器和药品:试管、滴管、带导管的单孔塞、蒸馏水、自来水、品红溶液、1 mol·L-1 HCl溶液、新制澄清石灰水。(提示:不必检验Ca2+和Cl-。)
| | 实验步骤 | 预期现象与结论 |
| 步骤1 | 取少量上述漂白粉于试管中,先加入 溶解后,再把生成的气体通入 。 | 若 ,则假设1成立; 若 ,则假设2或假设3成立。 |
| 步骤2 | 已确定漂白粉变质,则另取少量上述漂白粉于试管中,先加入适量1 mol·L-1 HCl溶液,再加入 。 | 若 ,则假设2成立; 若 ,则假设3成立。 |
(1)B A C D E(2分) 饱和食盐水(2分)
(2)2Cl2+2Ca(OH)2===CaCl2+Ca(ClO)2+2H2O(3分)
(3)①CaCO3(1分)
② 步骤1:适量1 mol?L-1盐酸(1分) 新制澄清石灰水中(1分)
澄清石灰水未见浑浊(1分) 澄清石灰水变浑浊(1分)
步骤2:几滴品红溶液 (1分) 品红溶液不褪色(1分) 品红溶液褪色(1分)
试题分析:制备氯气的实验中,要除去杂质氯化氢和水蒸汽,所以用到洗气装置,一般是长进短出,因此顺序为:B A C D E,又因为是先除去混合气中的氯化氢,因此广口瓶Ⅱ中的试剂为饱和食盐水,(氯气在饱和食盐水的溶解度较小)。。2、漂白粉的制备及有关性质。

练习册系列答案
相关题目