题目内容
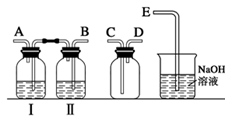
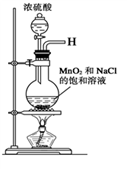
下列实验可行的是
| A.加入适量铜粉除去Cu(NO3)2溶液中的AgNO3杂质 |
| B.用NaOH溶液除去CO2中混有的HCl气体 |
| C.用浓硫酸与蛋白质反应的颜色变化鉴别部分蛋白质 |
| D.用乙醇从碘水中萃取碘 |
A
试题分析:A、铜与硝酸银溶液反应生成硝酸铜和单质银,因此可以除去硝酸铜溶液中的硝酸银,A正确;B、氢氧化钠溶液也能吸收CO2,B不正确,应该用饱和碳酸氢钠溶液除去CO2中混有的HCl气体;C、与蛋白质发生颜色反应的是浓硝酸,因此用浓硝酸与蛋白质反应的颜色变化鉴别部分蛋白质,C不正确;D、乙醇与水互溶,不能用乙醇从碘水中萃取碘,应该用四氯化碳或苯,D不正确,答案选A。

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目