题目内容
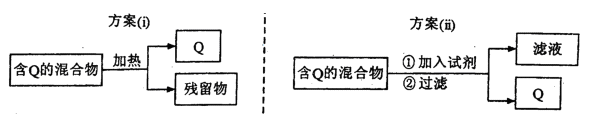
将草酸(H2C2O4)晶体粗品经①加热溶解、②趁热过滤、③冷却结晶、④过滤洗涤、⑤干燥等实验步骤,得到较纯净的草酸晶体。该过程中除去粗品中溶解度较大的杂质是在
| A.步骤②的滤液中 | B.步骤③的晶体中 | C.步骤④的滤液中 | D.步骤④的滤纸上 |
C
试题分析:草酸晶体在趁热过滤时可除去溶解度较小的杂质,在经冷却结晶、过滤洗涤后,滤液中含有溶解度较大的杂质。所以由操作顺序可知,草酸晶体粗品在经①加热溶解、②趁热过滤,可除去溶解度较小的杂质,然后③冷却结晶、④过滤洗涤,可除去溶解度较大的杂质,得到较为纯净的草酸晶体,所以答案选C。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目