题目内容
11.在密闭容器内放入5molH2和5molN2,在某温度下经过反应生成2molNH3,此时密闭容器内压强是反应前压强的( )| A. | 2倍 | B. | 1.5倍 | C. | 0.8倍 | D. | 0.5倍 |
分析 根据生成氨气物质的量计算反应后混合气体物质的量,反应前后混合气体的物质的量之比等于其压强之比,据此计算反应前后压强之比,据此分析解答.
解答 解:氢气和氮气反应方程式为N2(g)+3H2(g)?2NH3(g),根据方程式知,设反应前后气体物质的量减少为x,
N2(g)+3H2(g)?2NH3(g) 物质的量减少
2mol 2mol
2mol x
2mol:2mol=2mol:x
x=$\frac{2mol×2mol}{2mol}$=2mol,
则反应后混合气体物质的量=(5+5-2)=8mol,反应前混合气体物质的量=(5+5)mol=10mol,反应前后混合气体的物质的量之比等于其压强之比,所以此时密闭容器内压强是反应前压强=$\frac{8mol}{10mol}$=0.8,故选C.
点评 本题考查根据方程式进行计算,侧重考查学生分析计算能力,明确物质的压强与物质的量的关系即可解答,采用差量法解答,题目难度不大.

练习册系列答案
相关题目
2.某有机物X的结构简式如图所示,则下列有关说法中正确的是:( )
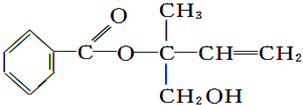

| A. | X的分子式为C12H16O3 | |
| B. | 可用酸性高锰酸钾溶液区分苯和X | |
| C. | X在一定条件下能发生水解、酯化、加成等反应 | |
| D. | 在Ni作催化剂的条件下,1 mol X最多只能与1 mol H2加成 |
19.下列各组物质中,属于同系物的是( )
| A. | 苯和丙苯 | B. | 乙苯和间二甲苯 | C. | 丁二烯和丁烯 | D. | 萘和苯 |
6.下列有关化学用语表示正确的是( )
| A. | 二氧化碳分子的结构式:O-C-O | |
| B. | 氢氧根离子的电子式: | |
| C. | 氯原子的结构示意图: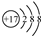 | |
| D. | 中子数为146、质子数为92 的铀(U)原子${\;}_{92}^{146}$U |
20.工业上可用黄铜矿(CuFeS2)冶炼铜,同时还可得到多种物质.工业冶炼铜的化学方程式是:8CuFeS2+2lO2 $\frac{\underline{\;高温\;}}{\;}$8Cu+4FeO+2Fe2O3+16SO2
(1)CuFeS2中Fe的化合价为+2,反应中被还原的元素是氧元素和铜元素.
(2)用少量黄铜矿冶炼铜产生的炉渣(主要含Fe2O3、FeO、SiO2、Al2O3)模拟制铁红(Fe2O3),进行如下实验.
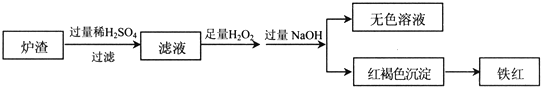
①滤液中的阳离子有Fe3+、Fe2+、H+、Al3+.
②为确认滤液中含Fe2+,下列实验方案和预期现象正确的是c(填序号).
③滤液在酸性条件下,与H2O2反应的离子方程式是2Fe2++H2O2+2H+=2Fe3++2H2O.
(3)冶炼铜过程中产生大量的SO2可用于制硫酸,尾气可用纯碱溶液吸收.已知用1L1mol/L的纯碱溶液吸收SO2,生成n(Na2SO3):n(NaHSO3)=1:2,则吸收的SO2物质的量是1.5mol.
(1)CuFeS2中Fe的化合价为+2,反应中被还原的元素是氧元素和铜元素.
(2)用少量黄铜矿冶炼铜产生的炉渣(主要含Fe2O3、FeO、SiO2、Al2O3)模拟制铁红(Fe2O3),进行如下实验.

①滤液中的阳离子有Fe3+、Fe2+、H+、Al3+.
②为确认滤液中含Fe2+,下列实验方案和预期现象正确的是c(填序号).
| 实验方案 | 预期现象 | |
| a | 加NaOH溶液 | 产生白色沉淀,变灰绿再变红褐 |
| b | 先加KSCN溶液,再加氯水 | 先无明显现象,后变红 |
| C | 加酸性KMnO4溶液 | 紫色褪去 |
| d | 先加氯水,再加KSCN溶液 | 溶液先变黄,再变红 |
(3)冶炼铜过程中产生大量的SO2可用于制硫酸,尾气可用纯碱溶液吸收.已知用1L1mol/L的纯碱溶液吸收SO2,生成n(Na2SO3):n(NaHSO3)=1:2,则吸收的SO2物质的量是1.5mol.
1.室温时,将浓度和体积分别为c1、V1的NaOH溶液和c2、V2的CH3COOH溶液相混合,下列关于该混合溶液的叙述错误的是( )
| A. | 在任何情况下都是c(Na+)+c(H+)=c(CH3COO-)+c(OH-) | |
| B. | 若pH>7,则一定是 c${\;}_{{1}_{\;}}$v1=c2v2 | |
| C. | 当pH=7时,若v1=v2,则一定是c2>c1 | |
| D. | 若v1=v2,c2=c1,则 c(CH3COO-)+c(CH3COOH)=c(Na+) |