题目内容
【题目】摩尔盐在工业上有重要的用途。已知其由一种阴离子,两种阳离子组成的晶体,某学习小组按如下实验测定摩尔盐样品的组成。步骤如下:
①称取3.920g摩尔盐样品配制250mL溶液。
②取少量配制溶液,加入KSCN溶液,无明显现象。
③另取少量配制溶液,加入过量浓氢氧化钠溶液并加热,产生使湿润的红色石蕊试纸变蓝的气体和红褐色沉淀。
④定量测定如下:
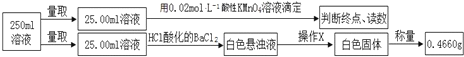
滴定实验结果记录如下:
实验次数 | 第一次 | 第二次 | 第三次 |
消耗高锰酸钾溶液体积/mL | 10.32 | 10.02 | 9.98 |
完成下列填空:
(1)步骤①中需要的定量仪器为________________ 、__________________。
(2)步骤②的目的是_____________________________________________________。产生红褐色沉淀的离子方程式_____________________________________。
(3)步骤④中操作X为_________________________________(按操作顺序填写)。
(4)步骤④中酸性高锰酸钾溶液能否用碘的酒精溶液代替,_______(填“能”或“不能”),请说明理由__________________________________________________。
(5)步骤④若在滴定过程中,待测液久置,消耗高锰酸钾溶液的体积将__________。(选填“ 偏大”、“偏小”或“不变”)。
(6)通过上述实验测定结果,推断摩尔盐化学式为______________________________。
【答案】电子天平 250mL容量瓶 确定红褐色沉淀中的铁元素在摩尔盐中是以亚铁离子形式存在 4Fe2++8OH-+O2+2H2O=4Fe(OH)3↓ 过滤、洗涤、干燥或烘干(冷却) 不能 碘单质与亚铁离子不反应 偏小 (NH4)2SO4FeSO46H2O或(NH4)2Fe(SO4)26H2O
【解析】
(1)配制摩尔盐溶液时,称取3.9200g摩尔盐样品要用电子天平称取,根据装置图可知,配制250mL溶液定容时要用250mL容量瓶;
(2)②取少量配制溶液,加入KSCN溶液,无明显现象,证明无铁离子存在,确定红褐色沉淀中的铁元素在摩尔盐中是以亚铁离子形式存在,产生红褐色沉淀的离子方程式为:4Fe2++8OH-+O2+2H2O=4Fe(OH)3↓;
(3)根据实验二③中操作流程可知,白色悬浊液为硫酸钡,要精确称量硫酸钡的质量要经过过滤、洗涤、干燥再称量;
(4)步骤④中酸性高锰酸钾溶液不能用碘的酒精溶液代替,因为碘单质和亚铁离子不发生反应,不能测定实验;
(5)步骤④若在滴定过程中,待测液久置,空气中氧气氧化亚铁离子,消耗标准溶液高锰酸钾溶液体积减小,c(待测)=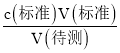 可知测定亚铁离子减小,故答案为偏小;
可知测定亚铁离子减小,故答案为偏小;
(6)根据题中实验步骤及数据可知,滴定亚铁离子用去的高锰酸钾溶液的体积的数据中,第一次误差较大,为偶然误差应去掉,所以高锰酸钾溶液的体积为![]() mL=10.00mL,高锰酸钾的物质的量为0.02mol/L×0.01L=0.0002mol,根据反应MnO4﹣+5Fe2++8H+=Mn2++5Fe3++4H2O,可知3.9200g摩尔盐样品中亚铁离子的物质的量为0.0002mol×
mL=10.00mL,高锰酸钾的物质的量为0.02mol/L×0.01L=0.0002mol,根据反应MnO4﹣+5Fe2++8H+=Mn2++5Fe3++4H2O,可知3.9200g摩尔盐样品中亚铁离子的物质的量为0.0002mol×![]() ×5=0.01mol,其质量为0.5600g,白色固体硫酸钡为0.4660g,所以3.9200g摩尔盐样品中硫酸根离子的物质的量为
×5=0.01mol,其质量为0.5600g,白色固体硫酸钡为0.4660g,所以3.9200g摩尔盐样品中硫酸根离子的物质的量为![]() ×
×![]() =0.02mol,其质量为1.9200g,根据电荷守恒可知3.9200g摩尔盐样品中铵根离子的物质的量为0.02mol×2﹣0.01mol×2=0.02mol,其质量为0.3600g,所以样品中结晶水物质的量为
=0.02mol,其质量为1.9200g,根据电荷守恒可知3.9200g摩尔盐样品中铵根离子的物质的量为0.02mol×2﹣0.01mol×2=0.02mol,其质量为0.3600g,所以样品中结晶水物质的量为![]() =0.06mol,所以摩尔盐的组成为(NH4)2SO4FeSO46H2O或(NH4)2Fe(SO4)26H2O。
=0.06mol,所以摩尔盐的组成为(NH4)2SO4FeSO46H2O或(NH4)2Fe(SO4)26H2O。