题目内容
【题目】请按要求回答下列问题:
(1)某气态有机物相对于氢气的密度为14,则其结构简式为____________。
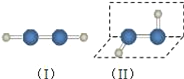
(2)某有机物的结构简式如图所示,则其一氯代物共有_______种。

(3)新戊烷用系统命名法命名应为_______。
(4)分别将等物质的量的C3H8、C4H8完全燃烧,消耗氧气质量多的是______(填分子式)。
(5)下列最简式中,只能代表一种有机物的有________(选填对应的序号)。
①CH3 ②CH2 ③CH2O ④CH4O
【答案】CH2=CH2 2 2,2-二甲基丙烷 C4H8 ①④
【解析】
(1)利用阿伏加德罗定律的推论,计算有机物的摩尔质量,结合相对分子质量分析气态有机物的分子结构;
(2)根据位置判断等效H的种类,以此可确定有机物的一氯代物种类,以此解答该题;
(3)根据新戊烷的结构式 分析命名;
分析命名;
(4)相同物质的量的烃CxHy完全燃烧,耗氧量取决于(x+![]() ),(x+
),(x+![]() )的值越大,耗氧量越多,据此判断;
)的值越大,耗氧量越多,据此判断;
(5)根据有机物中碳原子的饱和度分析判断;
(1)根据阿伏伽德罗定律的推论,同温同压下,气体的密度之比等于其摩尔质量之比。该气体有机物相对氢气的密度为14,则气体的摩尔质量=14×2g/mol=28g/mol,即相对分子质量为28,气态烃的衍生物中甲醛的相对分子质量最小,为30,则该气态有机物为烃类,气态烃中相对分子质量为28的只有乙烯,故结构简式为CH2=CH2;
(2)有机物 的等效氢如图:
的等效氢如图: ,则有机物的一氯代物有2种;
,则有机物的一氯代物有2种;
(3)新戊烷的结构简式为: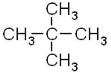 用系统命名法命名应为2,2-二甲基丙烷;
用系统命名法命名应为2,2-二甲基丙烷;
(4)相同物质的量的烃CxHy完全燃烧,耗氧量取决于(x+![]() ),(x+
),(x+![]() )的值越大,耗氧量越多,1molC3H8完全燃烧时的耗氧量为3+
)的值越大,耗氧量越多,1molC3H8完全燃烧时的耗氧量为3+![]() =5mol;1mol C4H8完全燃烧时的耗氧量为4+
=5mol;1mol C4H8完全燃烧时的耗氧量为4+![]() =6mol,故耗氧量多的为C4H8;
=6mol,故耗氧量多的为C4H8;
(5)最简式为CH3的烃其化学式一定为C2H6,CH4O的化学式为CH3OH,因为此时氢原子或其他原子数已经使碳原子达“饱和”状态,而其他选项的最简式,不知道相对原子质量,无法确定分子式,则能确定分子式的为①④。

 小学教材完全解读系列答案
小学教材完全解读系列答案【题目】摩尔盐在工业上有重要的用途。已知其由一种阴离子,两种阳离子组成的晶体,某学习小组按如下实验测定摩尔盐样品的组成。步骤如下:
①称取3.920g摩尔盐样品配制250mL溶液。
②取少量配制溶液,加入KSCN溶液,无明显现象。
③另取少量配制溶液,加入过量浓氢氧化钠溶液并加热,产生使湿润的红色石蕊试纸变蓝的气体和红褐色沉淀。
④定量测定如下:

滴定实验结果记录如下:
实验次数 | 第一次 | 第二次 | 第三次 |
消耗高锰酸钾溶液体积/mL | 10.32 | 10.02 | 9.98 |
完成下列填空:
(1)步骤①中需要的定量仪器为________________ 、__________________。
(2)步骤②的目的是_____________________________________________________。产生红褐色沉淀的离子方程式_____________________________________。
(3)步骤④中操作X为_________________________________(按操作顺序填写)。
(4)步骤④中酸性高锰酸钾溶液能否用碘的酒精溶液代替,_______(填“能”或“不能”),请说明理由__________________________________________________。
(5)步骤④若在滴定过程中,待测液久置,消耗高锰酸钾溶液的体积将__________。(选填“ 偏大”、“偏小”或“不变”)。
(6)通过上述实验测定结果,推断摩尔盐化学式为______________________________。