题目内容
【题目】下列说法正确的是( )
①难溶电解质达到沉淀溶解平衡时,溶液中各种离子的溶解(或沉淀)速率都相等
②难溶电解质达到沉淀溶解平衡时,增加难溶电解质的量,平衡向溶解方向移动
③向Na2SO4溶液中加入过量的BaCl2溶液,则![]() 沉淀完全,溶液中只含Ba2+、Na+和Cl-,不含
沉淀完全,溶液中只含Ba2+、Na+和Cl-,不含![]()
④Ksp小的物质其溶解能力一定比Ksp大的物质的溶解能力小
⑤为减少洗涤过程中固体的损耗,最好选用稀H2SO4代替H2O来洗涤BaSO4沉淀
⑥洗涤沉淀时,洗涤次数越多越好
A.①②③B.①②③④⑤⑥C.⑤D.①⑤⑥
【答案】C
【解析】
①难溶电解质达到沉淀溶解平衡时,溶液中各种离子的溶解(或沉淀)速率不一定相等,这与化学计量数有关,①不正确;
②难溶电解质达到沉淀溶解平衡时,增加难溶电解质的量,并未改变溶液中离子的浓度,对平衡不产生影响,②不正确;
③向Na2SO4溶液中加入过量的BaCl2溶液,![]() 仍未沉淀完全,因为达沉淀溶解平衡时,溶液中不仅含Ba2+、Na+和Cl-,还含
仍未沉淀完全,因为达沉淀溶解平衡时,溶液中不仅含Ba2+、Na+和Cl-,还含![]() ,③不正确;
,③不正确;
④同种类型的难溶电解质,Ksp越小,其溶解能力越小,但不同类型的难溶电解质,Ksp小,其溶解能力不一定小,④不正确;
⑤因为稀H2SO4中含有SO42-,可抑制BaSO4的溶解,所以为减少洗涤过程中固体的损耗,最好选用稀H2SO4代替H2O来洗涤BaSO4沉淀,⑤正确;
⑥洗涤沉淀时,洗涤次数越多,沉淀损失的越多,⑥不正确。
综合以上分析,只有⑤符合题意。故选C。

【题目】摩尔盐在工业上有重要的用途。已知其由一种阴离子,两种阳离子组成的晶体,某学习小组按如下实验测定摩尔盐样品的组成。步骤如下:
①称取3.920g摩尔盐样品配制250mL溶液。
②取少量配制溶液,加入KSCN溶液,无明显现象。
③另取少量配制溶液,加入过量浓氢氧化钠溶液并加热,产生使湿润的红色石蕊试纸变蓝的气体和红褐色沉淀。
④定量测定如下:
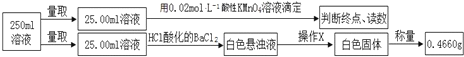
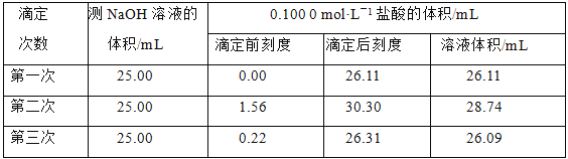
滴定实验结果记录如下:
实验次数 | 第一次 | 第二次 | 第三次 |
消耗高锰酸钾溶液体积/mL | 10.32 | 10.02 | 9.98 |
完成下列填空:
(1)步骤①中需要的定量仪器为________________ 、__________________。
(2)步骤②的目的是_____________________________________________________。产生红褐色沉淀的离子方程式_____________________________________。
(3)步骤④中操作X为_________________________________(按操作顺序填写)。
(4)步骤④中酸性高锰酸钾溶液能否用碘的酒精溶液代替,_______(填“能”或“不能”),请说明理由__________________________________________________。
(5)步骤④若在滴定过程中,待测液久置,消耗高锰酸钾溶液的体积将__________。(选填“ 偏大”、“偏小”或“不变”)。
(6)通过上述实验测定结果,推断摩尔盐化学式为______________________________。