题目内容
(9分)在2 L密闭容器内,800℃时反应2SO2(g)+O2(g) 2SO3(g)体系中,n(SO2)随时间的变化如下表:
2SO3(g)体系中,n(SO2)随时间的变化如下表:
(1)上述反应________(填“是”或“不是”)可逆反应,在第 5 s时,SO2的转化率为________;
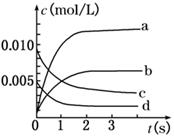
(2)如图所示,表示SO3变化曲线的是_____,用O2表示从0 s~2 s内该反应的平均速率:v=__;
(3)能说明该反应已达到平衡状态的是________。
a.v(SO3)=2v(O2) b.混合气体中SO2的体积分数保持不变
c.v逆(SO2)=2v正(O2) d.容器内密度保持不变
 2SO3(g)体系中,n(SO2)随时间的变化如下表:
2SO3(g)体系中,n(SO2)随时间的变化如下表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(SO2)(mol) | 0.020 | 0. 010 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)如图所示,表示SO3变化曲线的是_____,用O2表示从0 s~2 s内该反应的平均速率:v=__;

(3)能说明该反应已达到平衡状态的是________。
a.v(SO3)=2v(O2) b.混合气体中SO2的体积分数保持不变
c.v逆(SO2)=2v正(O2) d.容器内密度保持不变
(1)是(1分) 65﹪ (2分) (2)b(2分)0.0015 mol·L-1·s-1(2分) (3)bc(2分)
试题分析:(1)根据表中数据可知,反应进行到3s时SO2的物质的量不再发生变化,即SO2不能完全转化为三氧化硫,因此该反应是可逆反应。第5s时消耗三氧化硫的物质的量是0.020mol-0.007mol=0.013mol,所以此时SO2的转化率为
 ×100%=65%。
×100%=65%。(2)三氧化硫是生成物,平衡时生成三氧化硫的物质的量是0.013mol,其浓度为0.013mol÷2L=0.0065mol/L,所以根据图像可知,表示SO3变化曲线的是b。0 s~2 s内消耗SO2的物质的量是0.020mol-0.008mol=0.012mol,则根据方程式可知消耗氧气的物质的量是0.006mol,其浓度为0.003mol/L,则用O2表示从0 s~2 s内该反应的平均速率:v=0.003mol/L÷2s=0.0015 mol·L-1·s-1。
(3)在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态,则a.v(SO3)=2v(O2)符合反应速率之比是相应的化学计量数之比,但不能确定反应速率的方向,不能说明达到平衡状态,a不正确;b.混合气体中SO2的体积分数保持不变能说明达到平衡状态,b正确;c.v逆(SO2)=2v正(O2) 符合反应速率之比是相应的化学计量数之比,且反应速率的方向相反,能说明达到平衡状态,c正确;d.密度是混合气的质量和容器容积的比值,在反应过程中质量和容积始终是不变的,因此容器内密度保持不变不能说明反应达到平衡状态,d不正确,答案选bc。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
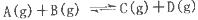 过程中的能量变化如图所示,下列说法错误的是
过程中的能量变化如图所示,下列说法错误的是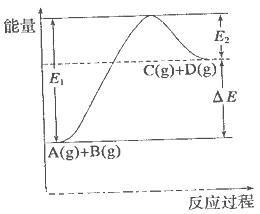
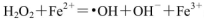
 ,则Fe2+在此过程中所起的作用是______________,当生成336mL O2(标准状况)时,反应中转移电子的物质的量为_______mol。
,则Fe2+在此过程中所起的作用是______________,当生成336mL O2(标准状况)时,反应中转移电子的物质的量为_______mol。
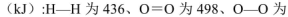
 .
. 2C
2C 4NO(g)+6HO(g) △H=-Q kJ· mol-1(Q>0),容器内部分物质的物质的量浓度如下表:
4NO(g)+6HO(g) △H=-Q kJ· mol-1(Q>0),容器内部分物质的物质的量浓度如下表: CH3OH(g)的平衡常数如下表。按照相同的物质的量投料,
CH3OH(g)的平衡常数如下表。按照相同的物质的量投料,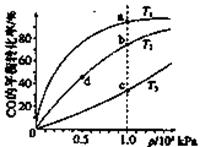
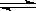 Z 在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述不正确的是 ( )
Z 在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述不正确的是 ( ) 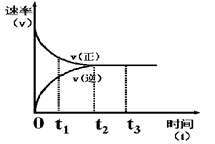
 x Q(g)+3R(g),经2min达平衡,生成2.4molR,并测得Q的浓度为0.4mol/L。求:
x Q(g)+3R(g),经2min达平衡,生成2.4molR,并测得Q的浓度为0.4mol/L。求: 2SO3(g),能增大正反应速率的措施是( )
2SO3(g),能增大正反应速率的措施是( )