题目内容
【题目】过氧化钙晶体![]() 较稳定,呈白色,微溶于水,能溶于酸性溶液
较稳定,呈白色,微溶于水,能溶于酸性溶液![]() 广泛应用于环境杀菌、消毒等领域。
广泛应用于环境杀菌、消毒等领域。
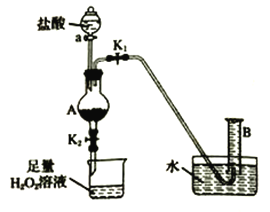
I.过氧化钙晶体的制备工业上生产![]() 的主要流程如下:
的主要流程如下:
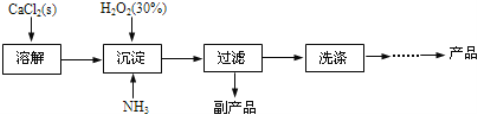
(1)用上述方法制取![]() 的化学方程式是 ____________________________________________________。
的化学方程式是 ____________________________________________________。
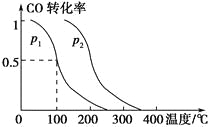
(2)沉淀时常用冰水控制温度在![]() 以下和通入过量的
以下和通入过量的![]() ,其可能原因分别是
,其可能原因分别是
①___________________________________;②__________________________________________.
II.过氧化钙晶体含量的测定
准确称取![]() 产品于锥形瓶中,加入30mL蒸馏水和
产品于锥形瓶中,加入30mL蒸馏水和![]() ,用
,用![]() 标准溶液滴定至终点
标准溶液滴定至终点![]() 重复上述操作两次。
重复上述操作两次。
③滴定终点观察到的现象为 _______________________________________________________________。
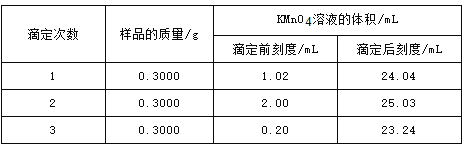
④根据表1数据,计算产品中![]() 的质量分数 ________________________。(保留四位有效数字)
的质量分数 ________________________。(保留四位有效数字)
表![]() 标准溶液滴定数据
标准溶液滴定数据
【答案】 ![]() 温度低可减少过氧化氢的分解,提高过氧化氢的利用率
温度低可减少过氧化氢的分解,提高过氧化氢的利用率![]() 或防止过氧化氢的分解
或防止过氧化氢的分解![]() 通入过量
通入过量![]() 使溶液呈碱性,抑制
使溶液呈碱性,抑制![]() 的溶解
的溶解![]() 或使溶液呈碱性,减少
或使溶液呈碱性,减少![]() 的溶解,或提高产品的产率
的溶解,或提高产品的产率![]() 当滴入最后一滴
当滴入最后一滴![]() 标准溶液后溶液由无色变浅红色,且30s不褪色 82.91%
标准溶液后溶液由无色变浅红色,且30s不褪色 82.91%
【解析】(1)题中所给工业流程中,利用氯化钙溶液、过氧化氢和氨气反应制备用上述方法制取![]() ,化学方程式是
,化学方程式是![]() 。
。
(2) ①过氧化氢不稳定,温度低可减少过氧化氢分解,提高过氧化氢利用率![]() 或防止过氧化氢的分解
或防止过氧化氢的分解![]() 。②.通入过量
。②.通入过量![]() 使溶液呈碱性,抑制
使溶液呈碱性,抑制![]() 的溶解
的溶解![]() 或使溶液呈碱性,减少
或使溶液呈碱性,减少![]() 的溶解,或提高产品的产率
的溶解,或提高产品的产率![]() 。
。
③滴定终点观察到的现象为:当滴入最后一滴![]() 标准溶液后溶液由无色变浅红色,且30s不褪色。
标准溶液后溶液由无色变浅红色,且30s不褪色。
④消耗KMnO4溶液的平均体积为23.03mL,由2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O得
5(![]() )~5H2O2~2KMnO4
)~5H2O2~2KMnO4
n(![]() )=
)=![]() n(KMnO4)=
n(KMnO4)=![]() ×0.0200mol/L×23.03mL×10-3L·mL-1=1.151×10-3mol
×0.0200mol/L×23.03mL×10-3L·mL-1=1.151×10-3mol
![]() 的质量分数为:1.151×10-3mol×216g·mol-1
的质量分数为:1.151×10-3mol×216g·mol-1![]() ×100%=82.91%
×100%=82.91%

 教学练新同步练习系列答案
教学练新同步练习系列答案