题目内容
18.物质X的结构式如图所示,常被用于香料或作为饮料的酸化剂.下列关于物质X的说法正确的是( )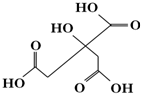
| A. | X分子式为C6H6O7 | |
| B. | 1 mol物质X可以和3 mol氢气发生加成 | |
| C. | X分子不可以发生消去反应 | |
| D. | 足量的X分别与等物质的量的NaHCO3、Na2CO3反应得到的气体物质的量相同 |
分析 由结构可知分子式,X在含3个-COOH、1个-OH,结合羧酸、醇的性质来解答.
解答 解:A.X分子式为C6H8O7,故A错误;
B.不能与氢气发生加成反应,故B错误;
C.与-OH相连C的邻位C上有H,可发生消去反应,故C错误;
D.-COOH与NaHCO3、Na2CO3反应,由C原子守恒可知,等物质的量的NaHCO3、Na2CO3反应得到的气体二氧化碳的物质的量相同,故D正确;
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握结构中官能团与性质的关系为解答的关键,侧重醇、羧酸等有机物性质的考查,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
7.下列各组物质中,其化学键类型完全相同的是( )
| A. | NH3和H2O | B. | HCl和KCl | C. | H2O和H2O2 | D. | NaCl和NaOH |
9.高锰酸钾是一种重要的化学试剂,其溶液不很稳定,在酸性条件下会分解生成二氧化锰和氧气,在中性或弱碱性溶液中分解速度很慢,见光分解速度加快.
(1)高锰酸钾溶液应配成中性溶液并保存在棕色试剂瓶中(填保存的注意事项);酸性条件下高锰酸钾溶液分解的离子方程式4MnO4-+4H+═4MnO2↓+3O2↑+2H2O.
(2)请配平高锰酸钾溶液与草酸钠Na2C2O4溶液在酸性条件下反应的离子方程式:MnO4-+C2O42-+H+--Mn2++CO2↑+8H2O
(3)某学习小组为了探究高锰酸钾溶液和草酸钠溶液的反应过程,将高锰酸钾溶液逐滴地滴入一定体积的酸性草酸钠溶液中(温度相同,并不断振荡时),记录的现象如表:
请分析高锰酸钾溶液褪色时间变化的原因反应生成的Mn2+对反应有催化作用,且c(Mn2+)浓度大催化效果更好.
(4)该学习小组在获取了上述经验和结论以后,用稳定的物质草酸钠Na2C2O4(相对分子质量134.0)来标定高锰酸钾溶液的浓度.他们准确称取1.340g纯净的草酸钠配成250mL溶液,每次准确量取25.00mL溶液酸化后用KMnO4溶液滴定.
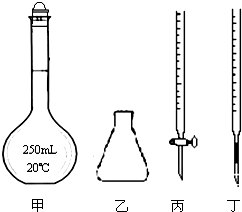
①高锰酸钾溶液应装在丙(填如图中的仪器编号).
②为了防止高锰酸钾在酸性条件下分解而造成误差,滴定时应注意的是逐滴滴入高锰酸钾溶液,待前一滴高锰酸钾溶液颜色褪去后再滴加.
③若在实验过程中存在下列操作,其中会使所测KMnO4浓度偏低的是A.
A.未润洗盛放KMnO4的滴定管
B.滴定前尖嘴部分无气泡,滴定终点时出现气泡
C.定容时,俯视刻度线
D.锥形瓶用水洗之后未用待测液润洗
④当溶液呈微红色且半分钟内不褪色,消耗KMnO4溶液20.00mL(多次测定的平均值),则KMnO4溶液的浓度为0.02mol/L.(附原子相对质量K=39 Mn=55 O=16 Na=23 C=12)

(1)高锰酸钾溶液应配成中性溶液并保存在棕色试剂瓶中(填保存的注意事项);酸性条件下高锰酸钾溶液分解的离子方程式4MnO4-+4H+═4MnO2↓+3O2↑+2H2O.
(2)请配平高锰酸钾溶液与草酸钠Na2C2O4溶液在酸性条件下反应的离子方程式:MnO4-+C2O42-+H+--Mn2++CO2↑+8H2O
(3)某学习小组为了探究高锰酸钾溶液和草酸钠溶液的反应过程,将高锰酸钾溶液逐滴地滴入一定体积的酸性草酸钠溶液中(温度相同,并不断振荡时),记录的现象如表:
滴入高锰酸钾溶液的次序(每滴溶液的体积相同) | 高锰酸钾溶液紫色褪去的时间 |
| 先滴入第1滴 | 1min |
| 褪色后再滴入第2滴 | 15s |
| 褪色后再滴入第3滴 | 3s |
| 褪色后再滴入第4滴 | 1s |
(4)该学习小组在获取了上述经验和结论以后,用稳定的物质草酸钠Na2C2O4(相对分子质量134.0)来标定高锰酸钾溶液的浓度.他们准确称取1.340g纯净的草酸钠配成250mL溶液,每次准确量取25.00mL溶液酸化后用KMnO4溶液滴定.
①高锰酸钾溶液应装在丙(填如图中的仪器编号).
②为了防止高锰酸钾在酸性条件下分解而造成误差,滴定时应注意的是逐滴滴入高锰酸钾溶液,待前一滴高锰酸钾溶液颜色褪去后再滴加.
③若在实验过程中存在下列操作,其中会使所测KMnO4浓度偏低的是A.
A.未润洗盛放KMnO4的滴定管
B.滴定前尖嘴部分无气泡,滴定终点时出现气泡
C.定容时,俯视刻度线
D.锥形瓶用水洗之后未用待测液润洗
④当溶液呈微红色且半分钟内不褪色,消耗KMnO4溶液20.00mL(多次测定的平均值),则KMnO4溶液的浓度为0.02mol/L.(附原子相对质量K=39 Mn=55 O=16 Na=23 C=12)
6.苯甲酸(C6H5COOH)是一种酸性比醋酸强的弱酸,下列说法不正确的是( )
| A. | 在水溶液中,C6H5COOH的电离方程式为:C6H5COOH?C6H5COO-+H+ | |
| B. | 0.1mol•L-1C6H5COONa溶液中离子浓度大小关系为:c(Na+)>c(C6H5COO-)>c(OH-)>c(H+) | |
| C. | C6H5COONa和C6H5COOH的混合溶液呈中性,且c(Na+)=0.1mol•L-1,则c(Na+)=c(C6H5COO-)>c(OH-)=c(H+) | |
| D. | 等浓度的C6H5COONa和CH3COONa两溶液中,前者离子总浓度小于后者 |
13.25℃时,下列叙述正确的是( )
| A. | NH4HSO4溶液中滴加NaOH溶液至pH=7,则c(Na+)=2c(SO42-) | |
| B. | 0.1 mol•L-1CH3COOH溶液与0.1 mol•L-1CH3COONa等体积混合pH<7,则c(CH3COO-)>c(Na+)>c(CH3COOH)>c(H+)>c(OH-) | |
| C. | AgCl在水中溶解度与在稀盐酸中溶解度相同 | |
| D. | KNO3溶液和CH3COONH4溶液pH均为7,则两溶液中水的电离程度相同 |
3.近年来我国很多城市发生严重的雾霾天气,对人们的健康造成严重威胁,下列有关环境问题的说法不正确的是( )
| A. | 改进汽车尾气净化技术,可以减少大气污染物的排放 | |
| B. | PM2.5是指大气中直径小于或等于2.5微米的颗粒物,与肺癌、哮喘等疾病的发生的发生密切相关,是雾霾天气的主要原因 | |
| C. | 推广燃煤脱硫技术可以降低SO2对大气的污染 | |
| D. | CO、SO2、NO、NO2都是对大气产生污染的气体,它们在空气中都能稳定存在 |
10.利用下列实验装置能 完成相应实验的是( )
| A. |  装置测定化学反应速率 | B. | 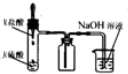 装置制取并吸收HCl | ||
| C. |  装置制备纯净NH3 | D. |  装置比较MnO2、Cl2、S |
7.有机物甲的分子式为C9H18O2,在酸性条件下甲水解为乙和丙两种有机物,在相同的温度和压强下,同质量的乙和丙的蒸气所占的体积相同,则甲可能的结构有( )
| A. | 12种 | B. | 14种 | C. | 16种 | D. | 18种 |

 ;其水溶液在空气中放置易变浑浊,写出反应的化学方程式2H2S+O2→2S↓+2H2O;该变化说明S的非金属性比O弱(填“强”或“弱”),从原子结构的角度解释原因:硫原子半径大于氧原子,硫原子的电子能力小于氧原子.通过H2O的稳定性大于H2S或SO2中硫是+4价,氧是-2价(举两例),也可以判断氧、硫两种元素的非金属性强弱.
;其水溶液在空气中放置易变浑浊,写出反应的化学方程式2H2S+O2→2S↓+2H2O;该变化说明S的非金属性比O弱(填“强”或“弱”),从原子结构的角度解释原因:硫原子半径大于氧原子,硫原子的电子能力小于氧原子.通过H2O的稳定性大于H2S或SO2中硫是+4价,氧是-2价(举两例),也可以判断氧、硫两种元素的非金属性强弱.