题目内容
2.已知在100℃的温度下,水的离子积KW=1×10-12(本题涉及的溶液温度均为100℃)下列说法正确的是( )| A. | 0.05 mol•L-1的H2SO4溶液pH=1 | |
| B. | 0.001 mol•L-1的NaOH溶液pH=11 | |
| C. | 0.005 mol•L-1的H2SO4溶液与0.01 mol•L-1的NaOH溶液等体积混合,混合溶液pH为6,溶液显酸性 | |
| D. | 完全中和pH=3的H2SO4溶液50 mL,需要pH=11的NaOH溶液50 mL |
分析 100℃的温度下,水的离子积KW=1×10-12,所以该温度下的中性溶液中pH=6,pH小于6的为酸性溶液,大于6的为碱性溶液,pH=-lgc(H+),强酸和强碱反应的混合溶液呈中性时,氢离子和氢氧根离子的物质的量相等,注意碱性溶液中氢氧根离子浓度的计算方法.
解答 解:100℃的温度下,水的离子积KW=1×10-12,所以该温度下的中性溶液中pH=6,
A.0.05 mol•L-1的硫酸溶液中,C(H+)=0.05 mol•L-1×2=0.1mol/L,所以pH=1,故A正确;
B.0.001mol/L的氢氧化钠溶液,C(H+)=10-9 mol/L,pH=9,故B错误;
C.0.005 mol•L-1的硫酸与0.01 mol•L-1的氢氧化钠溶液等体积时,n(H+)=n(OH-),所以硫酸和氢氧化钠恰好反应,溶液呈中性,pH为6,故C错误;
D.pH=3的硫酸中,C(H+)=10-3 mol/L,pH=11的NaOH溶液中C(OH-)=0.1mol/L,中和pH=3的硫酸溶液50 mL,需要pH=11的NaOH溶液0.5mL,故D错误;
故选A.
点评 本题考查pH的简单计算,注意碱性溶液中氢氧根离子浓度和pH的换算,为易错点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.某有机物A的分子式为C6H12O2,已知A~E有如图转化关系.则A的结构可能有( )
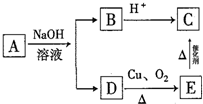

| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
10.葡萄糖的分子式为C6H12O6,其中氧的质量分数为是( )
| A. | 33.3% | B. | 25.0% | C. | 50.0% | D. | 53.3% |
17.下列有关化学用语表达不正确的是( )
| A. | 10个中子的氧原子的核素符号:${\;}_{8}^{18}$O | |
| B. | H2O分子的结构式:H-O-H | |
| C. | Na的原子结构示意图: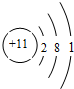 | |
| D. | 氮气的电子式::N:::N: |
11.已知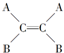 和
和 (A、B为不同的原子或原子团)互为同分异构体,称为烯烃的顺反异构.试推断一氯丙烯的同分异构体(不含环状结构)有( )
(A、B为不同的原子或原子团)互为同分异构体,称为烯烃的顺反异构.试推断一氯丙烯的同分异构体(不含环状结构)有( )
 和
和 (A、B为不同的原子或原子团)互为同分异构体,称为烯烃的顺反异构.试推断一氯丙烯的同分异构体(不含环状结构)有( )
(A、B为不同的原子或原子团)互为同分异构体,称为烯烃的顺反异构.试推断一氯丙烯的同分异构体(不含环状结构)有( )| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
12.共价键都有键能之说,键能是指拆开1mol共价键所需要吸收的能量或形成1mol共价键所放出的能量.
(1)已知H-Cl键的键能为431.4kJ/mol,下列关于键能的叙述正确的是AD.
A.每生成1mol H-Cl键放出431.4kJ能量
B.每生成1mol H-Cl键吸收431.4kJ能量
C.每拆开1mol H-Cl键放出431.4kJ能量
D.每拆开1mol H-Cl键吸收431.4kJ能量
(2)参考下表中的数据,判断下列分子受热时最稳定的是A.
A.HF B.HCl C.HBr D.H2
(3)能用键能大小解释的是A.
A.氮气的化学性质比氧气稳定
B.常温常压下,溴呈液态,碘呈固态
C.稀有气体一般很难发生化学反应
D.硝酸易挥发而硫酸难挥发
(4)已知:4HCl+O2═2Cl2+2H2O,该反应中,4mol HCl被氧化,放出115.6kJ的热量.断开1mol H-O键与断开1mol H-Cl键所需能量相差约为31.9kJ.
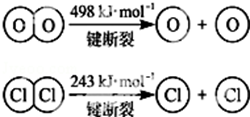
(1)已知H-Cl键的键能为431.4kJ/mol,下列关于键能的叙述正确的是AD.
A.每生成1mol H-Cl键放出431.4kJ能量
B.每生成1mol H-Cl键吸收431.4kJ能量
C.每拆开1mol H-Cl键放出431.4kJ能量
D.每拆开1mol H-Cl键吸收431.4kJ能量
(2)参考下表中的数据,判断下列分子受热时最稳定的是A.
| 化学键 | H-H | H-F | H-Cl | H-Br |
| 键能/kJ/mol | 436 | 565 | 431 | 368 |
(3)能用键能大小解释的是A.
A.氮气的化学性质比氧气稳定
B.常温常压下,溴呈液态,碘呈固态
C.稀有气体一般很难发生化学反应
D.硝酸易挥发而硫酸难挥发
(4)已知:4HCl+O2═2Cl2+2H2O,该反应中,4mol HCl被氧化,放出115.6kJ的热量.断开1mol H-O键与断开1mol H-Cl键所需能量相差约为31.9kJ.

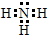


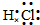
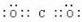
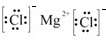 .
.
 .
.