题目内容
C、Si、Ge、Sn是同族元素,该族元素单质及其化合物在材料、医药等方面有重要应用.请回答下列问题:
(1)Ge的原子核外电子排布式为 .
(2)C、Si、Sn三种元素的单质中,能够形成金属晶体的是 .
(3)按要求指出下列氧化物的空间构型、成键方式或性质
①CO2分子的空间构型及碳氧之间的成键方式 ;
②SiO2晶体的空间构型及硅氧之间的成键方式 ;
③已知SnO2是离子晶体,写出其主要物理性质 (写出2条即可);
(4)CO可以和很多金属形成配合匆,如Ni(CO)4,Ni与CO之间的键型为 .
(5)碳氧键的红外伸缩振动频率与键的强度成正比,已知Ni(CO)4中碳氧键的伸缩振动频率为2060cm-1,CO分子中碳氧键的伸缩振动频率为2143cm-1,则Ni(CO)4中碳氧键的强度与CO分子中碳氧键的强度 (填字母).
A.强 B.弱 C.相等 D.无法判断.
(1)Ge的原子核外电子排布式为
(2)C、Si、Sn三种元素的单质中,能够形成金属晶体的是
(3)按要求指出下列氧化物的空间构型、成键方式或性质
①CO2分子的空间构型及碳氧之间的成键方式
②SiO2晶体的空间构型及硅氧之间的成键方式
③已知SnO2是离子晶体,写出其主要物理性质
(4)CO可以和很多金属形成配合匆,如Ni(CO)4,Ni与CO之间的键型为
(5)碳氧键的红外伸缩振动频率与键的强度成正比,已知Ni(CO)4中碳氧键的伸缩振动频率为2060cm-1,CO分子中碳氧键的伸缩振动频率为2143cm-1,则Ni(CO)4中碳氧键的强度与CO分子中碳氧键的强度
A.强 B.弱 C.相等 D.无法判断.
考点:同一主族内元素性质递变规律与原子结构的关系
专题:元素周期律与元素周期表专题
分析:(1)Ge是32号元素,其原子核外有32 个电子,根据构造原理书写其基态原子核外电子排布式;
(2)金属元素能形成金属晶体;
(3)①根据价层电子对互斥理论确定其空间构型,非金属元素之间易形成共价键;
②二氧化硅是原子晶体,每个硅原子和4个氧原子之间形成4个共价键,每个氧原子和2个硅原子形成2个共价键;非金属元素之间易形成共价键;
③熔融状态下,离子晶体能电离出阴阳离子,离子晶体的熔点与其晶格能成正比;
(4)含有空轨道和孤电子对的原子之间易形成配位键;
(5)碳氧键的红外伸缩振动频率与键的强度成正比.
(2)金属元素能形成金属晶体;
(3)①根据价层电子对互斥理论确定其空间构型,非金属元素之间易形成共价键;
②二氧化硅是原子晶体,每个硅原子和4个氧原子之间形成4个共价键,每个氧原子和2个硅原子形成2个共价键;非金属元素之间易形成共价键;
③熔融状态下,离子晶体能电离出阴阳离子,离子晶体的熔点与其晶格能成正比;
(4)含有空轨道和孤电子对的原子之间易形成配位键;
(5)碳氧键的红外伸缩振动频率与键的强度成正比.
解答:
解:(1)Ge是32号元素,其原子核外有32 个电子,根据构造原理知其基态原子核外电子排布式为1s22s22p63s23p63d104s24p2,
故答案为:1s22s22p63s23p63d104s24p2;
(2)金属元素能形成金属晶体,所以能形成金属晶体的是Sn,故答案为:Sn;
(3)①二氧化碳分子中碳原子价层电子对个数是2,且不含孤电子对,所以其空间构型是直线形,碳原子和氧原子之间存在共价键,故答案为:直线形、共价键;
②二氧化硅是原子晶体,Si-O通过共价键形成四面体结构,四面体之间通过共价键形成空间网状结构,硅原子和氧原子之间存在共价键,
故答案为:Si-O通过共价键形成四面体结构,四面体之间通过共价键形成空间网状结构;共价键;
③离子晶体在熔融状态下能电离呈自由移动的阴阳离子而导电,且离子晶体一般有较高的熔点,
故答案为:熔融时能导电、较高的熔点;
(4)镍原子中含有空轨道、CO中含有孤电子对,所以二者能形成配位键,故答案为:配位键;
(5)碳氧键的红外伸缩振动频率与键的强度成正比,已知Ni(CO)4中碳氧键的伸缩振动频率为2060cm-1,CO分子中碳氧键的伸缩振动频率为2143cm-1,则Ni(CO)4中碳氧键的强度与CO分子中碳氧键的强度弱,故选B.
故答案为:1s22s22p63s23p63d104s24p2;
(2)金属元素能形成金属晶体,所以能形成金属晶体的是Sn,故答案为:Sn;
(3)①二氧化碳分子中碳原子价层电子对个数是2,且不含孤电子对,所以其空间构型是直线形,碳原子和氧原子之间存在共价键,故答案为:直线形、共价键;
②二氧化硅是原子晶体,Si-O通过共价键形成四面体结构,四面体之间通过共价键形成空间网状结构,硅原子和氧原子之间存在共价键,
故答案为:Si-O通过共价键形成四面体结构,四面体之间通过共价键形成空间网状结构;共价键;
③离子晶体在熔融状态下能电离呈自由移动的阴阳离子而导电,且离子晶体一般有较高的熔点,
故答案为:熔融时能导电、较高的熔点;
(4)镍原子中含有空轨道、CO中含有孤电子对,所以二者能形成配位键,故答案为:配位键;
(5)碳氧键的红外伸缩振动频率与键的强度成正比,已知Ni(CO)4中碳氧键的伸缩振动频率为2060cm-1,CO分子中碳氧键的伸缩振动频率为2143cm-1,则Ni(CO)4中碳氧键的强度与CO分子中碳氧键的强度弱,故选B.
点评:本题考查了物质结构和性质,涉及知识点较多,这些知识点都是考试热点,知道配位键的形成条件、核外电子排布式的书写规则、价层电子对互斥理论的运用等知识点即可解答,知道计算价层电子对个数的方法,明确各个字母的含义,为学习难点.

练习册系列答案
相关题目
下列叙说正确的是( )
| A、一定温度下,若等浓度的NaA,NaB溶液,pH前者大于后者,则HA,HB的Ka前者小于后者 |
| B、在一定温度下的CaSO4的水溶液中,Ca2+和SO42-浓度的乘积是一定是常数 |
| C、常温时,浓度均为0.01mol/L Na2CO3溶液和NaHCO3溶液,等体积混合,其溶液中粒子浓度关系为3c(Na+)=2c(HCO3-)+2c(CO32-)+2c(H2CO3) |
D、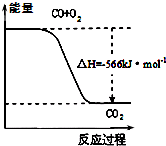 已知:2CO(g)+O2(g)=2CO2(g);△H=-566kJ?mol-1图可表示由CO生成CO2的反应过程和能量关系 |
下列说法正确的是( )
| A、不含其他杂质的天然油脂属于纯净物 |
| B、油脂在酸性或碱性条件下都比在纯水中易水解 |
| C、各种油脂水解后的产物中都有甘油 |
| D、油脂的烃基部分饱和程度越大,熔点越低 |
用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A、0.1mol Fe在过量的Cl2中充分燃烧,转移的电子数为0.3NA |
| B、常温下,22.4L甲烷中含有的共价键数目为4NA |
| C、2mol SO2和1mol O2在密闭容器中催化加热,充分反应后,容器内分子总数为2NA |
| D、由CO2和O2组成的混合气体中共有NA个分子,其中的氧原子数为2NA |
元素周期表中,划分周期的依据是( )
| A、元素的核电荷数 |
| B、元素原子的电子层数 |
| C、元素的化合价 |
| D、元素原子的最外层电子数 |
下列叙述正确的是( )
| A、加入铝粉能产生H2的溶液中可能大量共存的离子组:NH4+、Fe2+、SO42-、NO3- |
| B、碳酸氢钠溶液中离子浓度的大小关系c(Na+)>c(HCO3-)>c(OH-)>c(H+)>c(CO32-) |
| C、碳酸钠溶液中离子浓度的关系2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
| D、向Ca(ClO)2溶液中通入少量CO2的离子方程式:2ClO-+CO2+H2O═2HClO+CO32- |
下列微粒在溶液中能大量共存,通入SO2后仍能大量共存的一组是( )
| A、Ba2+、Na+、H+、Cl- |
| B、Na+、K+、SO32-、Cl- |
| C、Al3+、K+、Br-、HCO3- |
| D、Fe3+、Na+、H2O2、SO42- |
下列有关离子键、共价键的叙述中正确的是( )
| A、离子化合物中只存在离子键,没有共价键 |
| B、构成单质分子的粒子中一定含有共价键 |
| C、共价化合物分子中一定不存在离子键 |
| D、仅由非金属元素组成的化合物中一定不含离子键 |