题目内容
用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A、0.1mol Fe在过量的Cl2中充分燃烧,转移的电子数为0.3NA |
| B、常温下,22.4L甲烷中含有的共价键数目为4NA |
| C、2mol SO2和1mol O2在密闭容器中催化加热,充分反应后,容器内分子总数为2NA |
| D、由CO2和O2组成的混合气体中共有NA个分子,其中的氧原子数为2NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.铁与氯气反应生成氯化铁,0.1mol铁完全反应失去0.3mol电子;
B.常温下,不能使用标况下的气体摩尔体积计算甲烷的物质的量;
C.二氧化硫与氧气的催化氧化反应为可逆反应,反应物不可能完全转化成生成物;
D.二氧化碳和氧气分子中都含有2个氧原子,混合物中含有的氧原子数目为分子数目的2倍.
B.常温下,不能使用标况下的气体摩尔体积计算甲烷的物质的量;
C.二氧化硫与氧气的催化氧化反应为可逆反应,反应物不可能完全转化成生成物;
D.二氧化碳和氧气分子中都含有2个氧原子,混合物中含有的氧原子数目为分子数目的2倍.
解答:
解:A.0.1mol Fe在过量的Cl2中充分燃烧生成0.1mol氯化铁,转移了0.3mol电子,转移的电子数为0.3NA,故A正确;
B.常温下,不是标准状况下,题中条件无法计算22.4L甲烷的物质的量,故B错误;
C.2mol SO2和1mol O2在密闭容器中催化加热,由于该反应为可逆反应,反应生成三氧化硫的物质的量小于2mol,反应后容器内的分子的物质的量大于2mol,分子总数大于2NA,故C错误;
D.二氧化碳和氧气分子中都含有2个氧原子,若CO2和O2组成的混合气体中共有NA个分子,则含有的氧原子数为二氧化碳和氧气分子数的2倍,即氧原子数为2NA,故D正确;
故选AD.
B.常温下,不是标准状况下,题中条件无法计算22.4L甲烷的物质的量,故B错误;
C.2mol SO2和1mol O2在密闭容器中催化加热,由于该反应为可逆反应,反应生成三氧化硫的物质的量小于2mol,反应后容器内的分子的物质的量大于2mol,分子总数大于2NA,故C错误;
D.二氧化碳和氧气分子中都含有2个氧原子,若CO2和O2组成的混合气体中共有NA个分子,则含有的氧原子数为二氧化碳和氧气分子数的2倍,即氧原子数为2NA,故D正确;
故选AD.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系;选项C为易错点,注意可逆反应特点.

练习册系列答案
相关题目
下列物质中既含有离子键又含有共价键的化合物是( )
| A、NaCl |
| B、CH4 |
| C、KOH |
| D、CH3Cl |
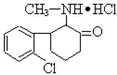 “K”粉医学上称氯胺酮,属于静脉全麻药品,具有一定的精神依赖性.因其物理形状通常为白色粉末,故称“K”粉.目前,该药物已被我国药检部门列为第二类精 神药品管理.其结构简式如下.
“K”粉医学上称氯胺酮,属于静脉全麻药品,具有一定的精神依赖性.因其物理形状通常为白色粉末,故称“K”粉.目前,该药物已被我国药检部门列为第二类精 神药品管理.其结构简式如下.下列说法正确的是( )
| A、“K”粉的化学式为C13H10NOCl2 |
| B、1mol“K”粉在一定条件下可与4mol H2发生加成反应 |
| C、“K”粉分子中至少有7个C原子处于同一平面 |
| D、“K”粉不能与NaOH溶液发生反应 |
推理是研究和学习化学的一种重要方法.以下推理正确的是( )
| A、酸碱发生中和反应生成盐和水,所以生成盐和水的反应一定是中和反应 |
| B、碱中都含有氢氧根,所以碱中一定含有氢元素 |
| C、酸能使紫色石蕊溶液变红,CO2通入紫色石蕊溶液后溶液变红,所以CO2是酸 |
| D、有机物都含碳元素,所以含碳元素的化合物都是有机物 |
(双项)在标准状况下,将2.24L NH3与4.48L HCl气体充入密闭容器内混合.已知:NH3+HCl═NH4Cl.下列说法正确的是( )
| A、反应中有0.5NA个共价键断裂 |
| B、反应中有0.1NA个离子键形成 |
| C、混合后,容器内物质含有0.5 NA个化学键 |
| D、混合前气体中含有0.5NA个共价键 |
元素M的最高正价和负价的绝对值之差为6,M、N的离子具有相同的电子排布,则M、N所形成的化合物可能是( )
| A、MgF2 |
| B、MgCl2 |
| C、CaCl2 |
| D、CaBr2 |
苯与乙烯相比较,下列叙述不正确的是( )
| A、都容易发生取代反应 |
| B、苯不能被KMnO4氧化 |
| C、苯只能在特殊条件下发生加成反应 |
| D、都能在空气中燃烧 |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、澄清透明的溶液中:Na+、K+、MnO4-、AlO2- | ||
| B、0.1mol?L-1 FeCl3溶液:K+、NH4+、I-、SCN- | ||
C、
| ||
| D、c(S2-)=0.1mol?L-1的溶液中:Na+、NH4+、ClO-、SO42- |