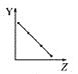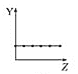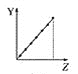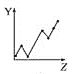题目内容
【题目】利用天然气水蒸气重整制备H2的反应为![]()
![]() 每次只改变一种条件(X),其它条件不变,CH4的平衡转化率
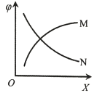
每次只改变一种条件(X),其它条件不变,CH4的平衡转化率![]() 随X的变化趋势如图所示。下列说法正确的是
随X的变化趋势如图所示。下列说法正确的是
A.某条件下,若CH4(g)、H2O(g)初始浓度均为0.2 mol/L,![]() = 25%,则K=3
= 25%,则K=3
B.X为投料比![]() 时,
时,![]() 的变化趋势为曲线N
的变化趋势为曲线N
C.X为压强时,![]() 的变化趋势为曲线M
的变化趋势为曲线M
D.X为温度时,![]() 的变化趋势为曲线N
的变化趋势为曲线N
【答案】B
【解析】
A.某条件下,若CH4(g)、H2O(g)初始浓度均为0.2 mol/L,![]() = 25%,则平衡后CH4(g)、H2O(g)、CO(g)、H2(g)的浓度分别为:0.15mol/L、0.15mol/L、0.05mol/L、0.15mol/L,则平衡常数K=
= 25%,则平衡后CH4(g)、H2O(g)、CO(g)、H2(g)的浓度分别为:0.15mol/L、0.15mol/L、0.05mol/L、0.15mol/L,则平衡常数K=![]() ,A选项错误;
,A选项错误;
B.X为投料比![]() 时,投料比增大,
时,投料比增大,![]() 减小,即
减小,即![]() 的变化趋势为曲线N,B选项正确;
的变化趋势为曲线N,B选项正确;
C.X为压强时,加压平衡逆向移动,![]() 减小,则
减小,则![]() 的变化趋势为曲线N,C选项错误;
的变化趋势为曲线N,C选项错误;
D.X为温度时,升高温度平衡正向移动,![]() 增大,则
增大,则![]() 的变化趋势为曲线M,D选项错误;
的变化趋势为曲线M,D选项错误;
答案选B。

 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案【题目】(1)通常人们把拆开1mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热(△H)。
化学键 | Si—O | Si—Cl | H—H | H—Cl | Si—Si | Si—C |
键能/kJ·mol—1 | 460 | 360 | 436 | 431 | 176 | 347 |
请回答下列问题:
①比较下列两组物质的熔点高低(填“>”或“<”=)
SiC_____________Si;SiCl4_____________SiO2
②工业上高纯硅可通过下列反应制取:SiCl4(g)+2H2(g)![]() Si(s)+4HCl(g)该反应的反应热△H=_____________kJ/mol.
Si(s)+4HCl(g)该反应的反应热△H=_____________kJ/mol.
(2)已知化合物Na2O的晶胞如图。
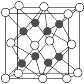
①其中O2-离子的配位数为________,
②该化合物与MgO相比,熔点较高的是________。(填化学式)
③已知该化合物的晶胞边长为apm,则该化合物的密度为___g·cm-3(只要求列出算式,不必计算出数值,阿伏加德罗常数的数值为NA)。
【题目】(I)某原料经测定主要含有A、B、C、D四种原子序数依次增大的短周期元素,其相关信息如下:
元素 | 元素性质或原子结构 |
A | 周期表中原子半径最小的元素 |
B | 原子核外有三种不同的能级且各个能级所填充的电子数相同 |
C | 最外层p轨道半充满 |
D | 位于短周期,其原子的核外成对电子数是未成对电子数的3倍 |
请回答下列问题(用A、B、C、D、所对应的元素符号作答):
(1) B、C、D第一电离能由大到小的顺序为__________________________________
(2)![]() 常用作除锈剂,该分子中B的杂化方式为_____;1 mol
常用作除锈剂,该分子中B的杂化方式为_____;1 mol ![]() 分子中含有σ键与π键的数目之比为_____。
分子中含有σ键与π键的数目之比为_____。
(3) ![]() 分子中均含有18个电子,它们的沸点相差较大,主要原因是_____________________
分子中均含有18个电子,它们的沸点相差较大,主要原因是_____________________
(Ⅱ)化学与生活密切相关。K2Cr2O7曾用于检测司机是否酒后驾驶:Cr2O![]() (橙色)+CH3CH2OH
(橙色)+CH3CH2OH![]() Cr3+(绿色)+CH3COOH (未配平)
Cr3+(绿色)+CH3COOH (未配平)
(4)基态Cr 原子的价电子排布图为__________________________________
(5)已知Cr3+等过渡元素水合离子的颜色如下表所示:
离子 | Sc3+ | Cr3+ | Fe2+ | Zn2+ |
水合离子的颜色 | 无色 | 绿色 | 浅绿色 | 无色 |
请根据原子结构推测Sc3+、Zn2+的水合离子为无色的原因为________________。
(6)ZnCl2浓溶液常用于除去金属表面的氧化物,例如与FeO反应可得Fe[Zn(OH)Cl2]2溶液。Fe[Zn(OH)Cl2]2的水溶液中不存在的粒子间作用力有____________(填选项字母);
A.离子键 B.共价键 C.金属键 D.配位键 E.范德华力 F.氢键
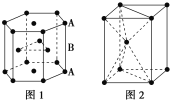
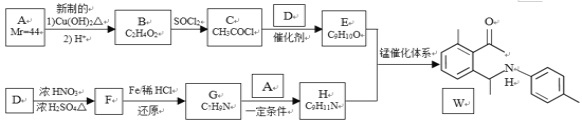
(7)锌是人体必需的微量元素之一,其堆积方式如图1,晶胞结构如图2。锌的堆积方式为_____________________,配位数为_______。