题目内容
8.已知可逆反应:aA(g)+bB(g)?cC(g)+dD(g),其中a,b,c,d为最简整数.(1)在密闭容器中将等物质的量的A、B、C、D四种气体混合,发生上述反应,当反应进行一段时间后测得A减少了n mol,B减少了$\frac{n}{2}$mol,C增加了$\frac{n}{2}$mol,D增加了$\frac{3n}{2}$mol,此时反应达到化学平衡状态,则a=2,b=1,c=1,d=3.
(2)取1mol A和2 molB置于2L密闭容器中,在一定条件下发生上述反应,5min后测得容器内D的浓度为0.3mol•L-1,5min末B的物质的量为1.8mol,这段时间内C的平均反应速率为0.02mol/(L.min).
(3)若该反应在恒温恒容条件下进行,则可作为判断该反应达到平衡状态的标志是②④(填序号)
①消耗a mol A,同时生产d mol D;
②D的百分含量保持不变;
③容器内气体的密度不再发生改变;
④v正(A)=$\frac{a}{c}$×v逆(C)
分析 (1)根据同一化学反应的同一时间段内,各物质的物质的量变化量之比等于其化学计量数之比;
(2)浓度变化量之比等于其化学计量数之比,根据D的浓度变化量计算B、C浓度变化量,根据△n=△c×V计算△n(B),进而计算5min末B的物质的量;根据v=$\frac{△c}{△t}$计算v(C);
(3)反应到达平衡时,同种物质表示的正、逆速率相等(不同物质表示的正、逆速率之比等于其化学计量之比),各组分的浓度、含量不变,由此衍生的一些其它量不变,选择判断平衡的物理量应随时间变化,该物理量由变化到不变化说明到达平衡,自始至终不变的物理量不能说明到达平衡.
解答 解:(1)同一化学反应的同一时间段内,各物质的物质的量变化量之比等于其化学计量数之比,则:a:b:c:d=n mol:$\frac{n}{2}$mol:$\frac{n}{2}$mol:$\frac{3n}{2}$mol=2:1:1:3,故a=2、b=1、c=1、d=3,
故答案为:2;1;1;3;
(2)5min后测得容器内D的浓度为0.3mol•L-1,则:△c(B)=$\frac{1}{3}$△c(D)=$\frac{1}{3}$×0.3mol/L=0.1mol/L,故△n(B)=△c×V=0.1mol/L×2L=0.2mol,故5min末B的物质的量为2mol-0.2mol=1.8mol;
△c(C)=$\frac{1}{3}$△c(D)=$\frac{1}{3}$×0.3mol/L=0.1mol/L,故v(C)=$\frac{△c}{△t}$=$\frac{0.1mol/L}{5min}$=0.02mol/(L.min),
故答案为:1.8mol;0.02mol/(L.min);
(3)①消耗a mol A,同时生产d mol D,均表示正反应速率,反应自始至终都按此比例进行,不能说明得到平衡,故错误;
②随反应进行D的含量增大,D的百分含量保持不变,说明反应到达平衡,故正确;
③混合气体总质量不变,容器容积不变,容器内气体的密度始终不变,不能说明到达平衡,故错误;
④v正(A)=$\frac{a}{c}$×v逆(C)即v正(A):v逆(C)=a:c,反应到达平衡,故正确,
故选:②④.
点评 本题考查化学平衡计算、反应速率计算、化学平衡状态的判断,难度不大,注意选择判断平衡的物理量应随时间变化,该物理量由变化到不变化说明到达平衡.

 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案①改变核外电子数可使原子与离子相互转化
②改变核内中子数可使不同的同位素相互转化
③改变核内质子数可使不同的元素相互转化,属于化学变化
④改变离子的电荷数可使一种元素的阳离子转化为另一种元素的阴离子.
| A. | ①② | B. | ②③ | C. | ③④ | D. | ①③ |
| A. | 4 | B. | 12 | C. | 16 | D. | 18 |
| A. | CH4 C2H4 C3H4 | B. | C2H6 C3H6 C4H6 | C. | CH4 C2H6 C3H8 | D. | C2H2 C2H6 C3H6 |
 为研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验,请回答下列问题.
为研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验,请回答下列问题.| 编号 | 操作 | 实验现象 |
| ① | 分别在试管A、B中加入 5mL 5% H2O2溶液,各滴入1~2 滴1mol/L FeCl3溶液.待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中;将试管B放入盛有40℃左右热水的烧杯中 | 试管A中不再产生气泡 试管B中产生的气泡量增大 |
| ② | 另取两支试管分别加入 5mL 5%H2O2溶液和 5mL10%H2O2溶液 | 试管A、B中均未见气泡产生 |
(2)实验②未观察到预期的实验现象,为了帮助该同学达到实验目的,你提出的对上述操作的改进意见是③(填序号).
①加热5%H2O2溶液 ②分别加入5mL5%H2O2③加入1~2 滴1mol/L FeCl3溶液
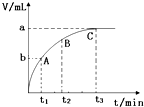
(3)某同学在50mL H2O2 溶液中加入一定量的二氧化锰,放出气体的体积(标准状况)与反应时间的关系如图所示,则A、B、C三点所表示的即时反应速率最慢的是C.
| A. | 用电子式表示溴化氢的形成过程为: | |
| B. | 海水中Br-的电子式为: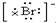 | |
| C. | 海水中通入氯气时发生反应的离子方程式为:2NaBr+Cl2=Br2+2NaCl | |
| D. | 氯离子的结构示意图为: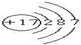 |
| A. | 同族元素,随着电子层的增加,I1逐渐增大 | |
| B. | 通常情况下,电离能I1<I2<I3 | |
| C. | 同周期元素,随着核电荷数的增加,I1呈增大趋势 | |
| D. | 电离能越小,元素的金属性越强 |





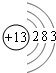 ,它的单质能(填能或不能)与氢氧化钠溶液反应.
,它的单质能(填能或不能)与氢氧化钠溶液反应.