��Ŀ����
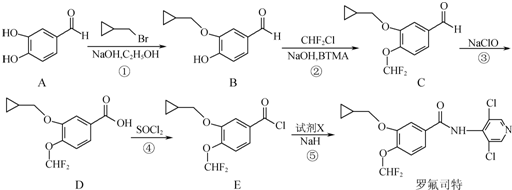
16����«����һ�ֿ�������ҩ��ϳ�����һ��·�����£�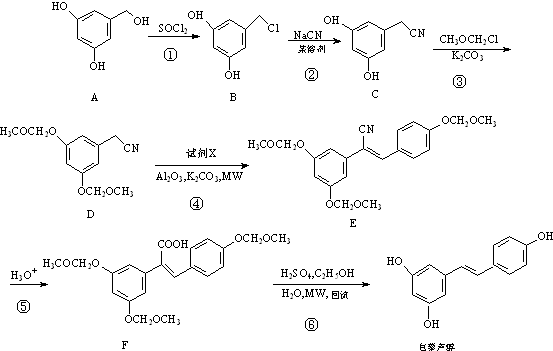
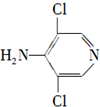
��1��������F�еĺ��������ŵ��������Ȼ����Ѽ���
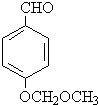
��2����Ӧ���м����Լ�X�ķ���ʽΪC9H10O3��X�Ľṹ��ʽΪ
 ��
����3���ڢ١��ܷ�Ӧ�У�����ȡ����Ӧ���Ǣ٢ڢۣ�����ţ���
��4��D��һ��ͬ���칹����������������
�����ڦ����������ʹ��ˮ��ɫ��������ʹFeCl3��Һ��ɫ����������7�ֲ�ͬ��ѧ�������⣬�ұ����ϵ�һȡ����ֻ��һ�֣�д����ͬ���칹��Ľṹ��ʽ��
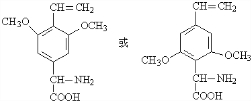 ����дһ�֣���
����дһ�֣�����5����������֪ʶ����������Ϣ��д������ȩΪԭ���Ʊ�CH3CH�TC��CH3��COOH�ĺϳ�·������ͼ�����Լ����ã����ϳ�·������ͼʾ�����£�H2C�TCH2$��_{��}^{HBr}$CH3CH2Br$��_{��}^{NaOH��Һ}$CH3CH2OH��
���� ��1����F�Ľṹ��ʽ��֪�����еĺ���������Ϊ�Ȼ����Ѽ���
��2����Ӧ���м����Լ�X�ķ���ʽΪC9H10O3���Ա�D��E�Ľṹ��X����ʽ��֪��D��X��ȥ1����ˮ�õ�E����D��-CN���ӵ��Ǽ���X��ȩ����ȥ1����ˮ�γ�̼̼˫�����õ�E��
��3����Ӧ����-Clȡ��-OH����������Ӧ����-CNȡ��-Cl����Ӧ���з��ǻ���Hԭ�ӱ�-OCH2OCH3ȡ������Ӧ�ܷ�����ˮ��Ӧͬʱ�γ�̼̼˫����������ȡ����Ӧ��
��4��D��һ��ͬ���칹���������������������ڦ�-�����ᣬ���а������Ȼ����Ҷ�������ͬһ̼ԭ���ϣ�
����ʹ��ˮ��ɫ��������ʹFeCl3��Һ��ɫ���������ǻ������Ժ���̼̼˫������������7�ֲ�ͬ��ѧ�������⣬�ұ����ϵ�һȡ����ֻ��һ�֣������Ϻ���1��Hԭ�ӣ������й�����6�ֲ�ͬ��Hԭ�ӣ�
��5����ȩ�����������ӳɷ�Ӧ�����Ҵ����Ҵ�����ת����ϵ�Тٵķ�Ӧ�õ�CH3CH2Cl���ٽ�Ϸ�Ӧ�ڵõ�CH3CH2CN����Ϸ�Ӧ�ܿ�֪��CH3CH2CN����ȩ��Ӧ�õ�CH3CH=C��CH3��CN���ٸ��ݷ�Ӧ�ݣ�CH3CH=C��CH3��CN�ữ�õ�CH3CH=C��CH3��COOH��
��� �⣺��1����F�Ľṹ��ʽ��֪�����еĺ���������Ϊ�Ȼ����Ѽ����ʴ�Ϊ���Ȼ����Ѽ���
��2����Ӧ���м����Լ�X�ķ���ʽΪC9H10O3���Ա�D��E�Ľṹ��X����ʽ��֪��D��X��ȥ1����ˮ�õ�E����D��-CN���ӵ��Ǽ���X��ȩ����ȥ1����ˮ�γ�̼̼˫�����õ�E������֪X�Ľṹ��ʽΪ�� ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��3���Ա����ʵĽṹ��֪����Ӧ����-Clȡ��-OH������������ȡ����Ӧ����Ӧ����-CNȡ��-Cl������ȡ����Ӧ����Ӧ���з��ǻ���Hԭ�ӱ�-OCH2OCH3ȡ��������ȡ����Ӧ����Ӧ�ܷ�����ˮ��Ӧͬʱ�γ�̼̼˫����������ȡ����Ӧ����ѡ���٢ڢۣ�
��4��D��һ��ͬ���칹���������������������ڦ�-�����ᣬ���а������Ȼ����Ҷ�������ͬһ̼ԭ���ϣ�
����ʹ��ˮ��ɫ��������ʹFeCl3��Һ��ɫ���������ǻ������Ժ���̼̼˫������������7�ֲ�ͬ��ѧ�������⣬�ұ����ϵ�һȡ����ֻ��һ�֣������Ϻ���1��Hԭ�ӣ������й�����6�ֲ�ͬ��Hԭ�ӣ�����������ͬ���칹��Ϊ �ȣ�
�ȣ�
�ʴ�Ϊ�� ��
��
��5����ȩ�����������ӳɷ�Ӧ�����Ҵ����Ҵ�����ת����ϵ�Тٵķ�Ӧ�õ�CH3CH2Cl���ٽ�Ϸ�Ӧ�ڵõ�CH3CH2CN����Ϸ�Ӧ�ܿ�֪��CH3CH2CN����ȩ��Ӧ�õ�CH3CH=C��CH3��CN���ٸ��ݷ�Ӧ�ݣ�CH3CH=C��CH3��CN�ữ�õ�CH3CH=C��CH3��COOH���ϳ�·������ͼΪ��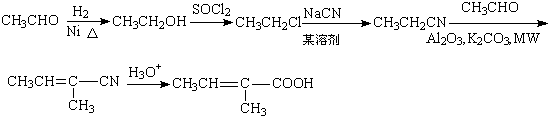 ��
��
�ʴ�Ϊ�� ��
��
���� ���⿼���л���ĺϳɣ�ע������л���Ľ��н��з�������漰�����ŵĽṹ���л���Ӧ���͡���������ͬ���칹����д���ϳ�·����Ƶȣ���5����ע������ת����ϵ����������Ϣ���ϺõĿ���ѧ������Ϣ��ȡ��Ǩ�����ã��Ѷ��еȣ�


��֪���ٲ��ֽ�����������ȫ����ʱ��pH���±�
| ���������� | Fe3+ | Al3+ | Mn2+ | Mg2+ |
| ��ȫ����ʱ��PHֵ | 3.2 | 5.2 | 10.4 | 12.4 |
��1����������������MnO2ת��ΪMn2+�����ӷ���ʽΪSO2+MnO2�TMn2++SO42-��
��2����1�������м���H2O2��Ŀ���ǽ�Fe2+����ΪFe3+��
��3����1���������γ�����l����Ҫ�ɷ�ΪAl��OH��3��Fe��OH��3���ѧʽ������pH��5-6���ӵ��Լ�����ѡ��a��b���������Լ��������ĸ���� a��Cao b��MgO c��Al2O3 d����ˮ
��4����2�����ӣ���Ҫ�ǽ�Ca2+��Mg2+ת��Ϊ��Ӧ�����������ȥ��д��MnF2��ȥMg2+�����ӷ�Ӧ����ʽMnF2+Mg2+�TMn2++MgF2���÷�Ӧ��ƽ�ⳣ����ֵΪ7.2��107��
����֪��MnF2��Ksp=5.3��10-3��CaF2��Ksp=1.5��10-10��MgF2��Ksp=7.4��10-11����
��5�����á����ȹ��ˡ�������ԭ������Ϊ����MnSO4•H2O��ˮ�е��ܽ⣬�õ������ò�Ʒ��
��6��ȡ����MnSO4•H2O����ˮ�������Һ������pH���ָ���Һ�����ԣ�ԭ����Mn2++2H2O?Mn��OH��2+2H+�������ӷ���ʽ��ʾ��������Һ���������ӵ�Ũ���ɴ�С��˳��Ϊc��SO42-����c��Mn2+����c��H+����c��OH-����
| ѡ�� | ʵ������ | ���� |
| A | ȡijNa2SO3��Һ������������ϡ���ᣬ�������ݣ��ٵμ�BaCl2��Һ��������ɫ������ | Na2SO3�Ѳ��ֱ����� |
| B | ��2mL0.1mol/LNaOH��Һ�еμ�0.1mol/LMgCl2��Һ3�Σ����ְ�ɫ�������ٵμ�3��0.1mol/L FeCl3��Һ�����ֺ��ɫ������ | �ܽ�ȣ�Mg��OH��2��Fe��OH��3 |
| C | ����ˮ��ͨ������SO2����ˮ��ɫ�� | SO2����Ư���� |
| D | ��ͬ�¶��£����Ũ�ȵ�Na2CO3��Na2SO3ˮ��Һ��pH��pH ��Na2CO3����pH��Na2SO3���� | �ǽ�����ǿ����C��S |
| A�� | A | B�� | B | C�� | C | D�� | D |
2CO��g��+O2��g���T2CO2��g����H2
2H2��g��+O2��g���T2H2O��l����H3
2H2��g��+O2��g���T2H2O��g����H4
CO��g��+2H2��g���TCH3OH��g����H5
���й���������Ӧ�ʱ���ж���ȷ���ǣ�������
| A�� | ��H1��0����H2��0 | B�� | ��H3����H4 | ||
| C�� | ��H1=��H2+2��H3-��H5 | D�� | 2��H5+��H1��0 |
| A�� | �������п����ǿ�俹��ʴ�� | |
| B�� | ������ά���ϳ���ά���ά�����������ǽ������� | |
| C�� | ����������������������θ������ҩ�� | |
| D�� | ��ú����������ú�ĵ硱�ȸ��칤�������ڼ����������� |
��1��������ˮ��Һ�д��ڵ���ƽ�⣬����0.1mol•L-1����ĵ���ƽ�ⳣ�����±���
| ���� | ����ƽ�ⳣ����25�棩 |
| HClO | K=2.98��10-8 |
| H2CO3 | K1=4.3��10-7 K2=5.6��10-11 |
| H2SO3 | K1=1.54��10-2 K2=1.02��10-7 |
���������ӷ���ʽ���й�˵���������ad
a��������CO2ͨ�����������Һ�У�2ClO-+H2O+CO2=2HClO+CO32-
b��������SO2ͨ��̼������Һ�У�SO2+H2O+2CO32-=2HCO3-+SO32-
c����ͬ�¶�ʱ����pH��������Һ�����ʵ���Ũ�ȹ�ϵ��c��Na2CO3����c��NaClO����c��Na2SO3��
d����ͬ�¶�ʱ�������ʵ�����������������NaOH��Һ��ȫ�к�����NaOH�����Ϊ��V��H2CO3����V��H2SO3����V��HClO��
�������ᣨH2SeO3��Ҳ��һ�ֶ�Ԫ���ᣬ�н�ǿ�������ԣ�����������Һ�в���ͨ��SO2��������ɫ���ʣ�д���÷�Ӧ�Ļ�ѧ����ʽ��H2SeO3+2SO2+H2O=Se��+2H2SO4���÷�Ӧ������������H2SO4��
��2����ҵ��ˮ�г�����һ������Cr2O72-��CrO42-�����Ƕ����༰��̬ϵͳ�����ܴ���������д������ŷţ�
���ڷ�ˮ�д���ƽ�⣺2CrO42-����ɫ��+2H+?Cr2O72-����ɫ��+H2O���ı�����ʹ����ƽ��������Ӧ�����ƶ���������˵����ȷ����ac
a��ƽ�ⳣ��Kֵ���Բ��ı�
b���ﵽ��ƽ��CrO42-���������ʵ���Cr2O72-����������
c���ٴ�ƽ��ǰ����Ӧ����һ�������淴Ӧ����
d��ƽ���ƶ���ﵽ��ƽ����ҺpHһ������
��Cr2O72-��CrO42-�������ɵ�Cr��OH��3����Һ�д������³����ܽ�ƽ�⣺Cr��OH��3��s��?Cr3+��aq��+3OH?��aq�������£�Cr��OH��3���ܶȻ�Ksp=c��Cr3+��•c3��OH-��=10-32����c��Cr3+������10-3 mol•L-1����Һ��pH����4ʱ��û�У���С���û�С�������������
��3����֪����CO��g��+2H2��g��?CH3OH��g��
��2CH3OH��g��?CH3OCH3��g��+H2O��g��
��CO��g��+H2O��g��?CO2��g��+H2��g��
ij�¶���������Ӧ��ƽ�ⳣ����ֵ����Ϊa1��a2��a3������¶��·�Ӧ 3CO��g��+3H2��g��?CH3OCH3��g��+CO2��g�� �Ļ�ѧƽ�ⳣ��K=a12•a2•a3L4•mol-4���ú�a1��a2��a3�Ĵ���ʽ��ʾ����
��ij�̶�������ܱ������м���3molCO��3molH2����ַ�Ӧ��ָ���ԭ���¶ȣ��ⶨ������ѹǿΪ��Ӧǰ��$\frac{2}{3}$����CO��ת����50%��
 ��
��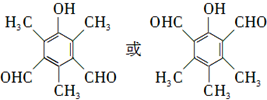 �ȣ�
�ȣ�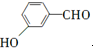 ��CH3CH2OHΪԭ���Ʊ�
��CH3CH2OHΪԭ���Ʊ�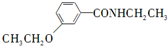 �ĺϳ�·������ͼ�����Լ����ã����ϳ�·������ͼʾ�����£�
�ĺϳ�·������ͼ�����Լ����ã����ϳ�·������ͼʾ�����£�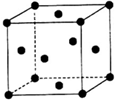 W��X��Y��Z��W��X��Y��Z�ֱ����Ԫ�ط��ţ���ΪԪ�����ڱ���ǰ�����ڵ�Ԫ�أ���ԭ������������������W��X��YΪ������Ԫ�أ����ǵĵ�����ͨ��״���¾�Ϊ��ɫ���壮XԪ�صĻ�̬ԭ����ͬ����Ԫ�ػ�̬ԭ���к��е�δ�ɶԵ�������࣬YԪ�صĻ�̬ԭ����s�ܼ��ϵĵ���������p�ܼ��ϵĵ�������ZΪ����Ԫ�أ����̬ԭ���Ǿ���4s1�ṹ�Ļ�̬ԭ��������������ԭ�ӣ��Իش����и��⣺
W��X��Y��Z��W��X��Y��Z�ֱ����Ԫ�ط��ţ���ΪԪ�����ڱ���ǰ�����ڵ�Ԫ�أ���ԭ������������������W��X��YΪ������Ԫ�أ����ǵĵ�����ͨ��״���¾�Ϊ��ɫ���壮XԪ�صĻ�̬ԭ����ͬ����Ԫ�ػ�̬ԭ���к��е�δ�ɶԵ�������࣬YԪ�صĻ�̬ԭ����s�ܼ��ϵĵ���������p�ܼ��ϵĵ�������ZΪ����Ԫ�أ����̬ԭ���Ǿ���4s1�ṹ�Ļ�̬ԭ��������������ԭ�ӣ��Իش����и��⣺