题目内容
【题目】聚合硫酸铝铁(PAFS)是一种高效净水剂,其组成表示为[AlFe(OH)x(SO4)(3-![]() )]y。为检测PAFS中Al的含量,设计如下流程。
)]y。为检测PAFS中Al的含量,设计如下流程。

回答下列问题:
(1)实验中需配制1.0mol/L的NaOH溶液100mL,所需仪器除了玻璃棒、托盘天平、量筒、药匙、烧杯、胶头滴管,还缺少的仪器为__。
(2)PAFS中铁元素的化合价为_______;沉淀A的化学式为_________。
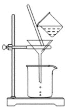
(3)如图所示,过滤操作中的一处错误是__________。
(4)生成沉淀B的离子方程式为______。
(5)PAFS中Al元素的质量分数为_______(用同m、n的代数式表示)。
【答案】100mL容量瓶 +3 Fe(OH)3 漏斗下端尖嘴未紧贴烧杯内壁 CO2+AlO2-+2H2O=Al(OH)3↓+HCO3-或CO2+2AlO2-+3H2O=2Al(OH)3↓+CO32-、CO2+CO32-+H2O=2HCO3- ![]() 或
或![]()
【解析】
为检测PAFS中Al含量,PAFS加入足量氢氧化钠溶液反应生成氢氧化铁沉淀和偏铝酸钠溶液,过滤后得到氢氧化铁,滤液中通入过量二氧化碳气体,生成氢氧化铝沉淀,灼烧得到氧化铝。
(1)配制1.0mol/L的NaOH溶液100mL,涉及称量、溶解、移液、洗涤、定容等操作,则需要的仪器有玻璃棒、托盘天平(量筒)、烧杯、胶头滴管,还需要100mL容量瓶,故答案为:100mL容量瓶;
(2)化学式为:[AlFe(OH)x(SO4)(3-![]() )]y,其中Al为+3价,设Fe的化合价为m,则3+m=x+2×(3-
)]y,其中Al为+3价,设Fe的化合价为m,则3+m=x+2×(3-![]() ),m=+3,沉淀A的化学式为:
),m=+3,沉淀A的化学式为:
Fe(OH)3,故答案为:+3;Fe(OH)3;
(3)过滤时,漏斗下端应紧贴烧杯内壁,避免液体飞溅,故答案为:漏斗下端尖嘴未紧贴烧杯内壁;
(4)偏铝酸钠溶液中通入过量二氧化碳气体生成氢氧化铝沉淀,反应的离子方程式:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-或2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-、CO2+CO32-+H2O=2HCO3-,故答案为:CO2+AlO2-+2H2O=Al(OH)3↓+HCO3-或2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-、CO2+CO32-+H2O=2HCO3-;
(5)m g PAFS生成n g氧化铝,铝的质量为:![]() g,则铝的含量为
g,则铝的含量为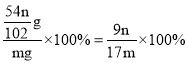 ,故答案为:
,故答案为:![]() 或
或![]() 。
。