题目内容
5.下列关于元素周期表和元素周期律的说法正确的是( )| A. | Li、Na、K元素的原子核外电子层数随着核电荷数的增加而减少 | |
| B. | 因为K比Na容易失去电子,所以K比Na的还原性强 | |
| C. | 第二周期元素从Li到F,非金属性逐渐减弱 | |
| D. | O与S为同主族元素,且O比S的非金属性弱 |
分析 A.同主族自上而下电子层增多,核电荷数增大;
B.金属性越强,金属越容易失去电子;
C.同周期自左而右元素金属性减弱、非金属性增强;
D.O与S为同主族元素,同主族自上而下元素非金属性减弱.
解答 解:A.Li、Na、K元素的原子核外电子层数随着核电荷数的增加而增多,故A错误;
B.金属越容易失去电子,则金属性越强,K比Na容易失去电子,所以K比Na的还原性强,故B正确;
C.第二周期元素从Li到F,金属性逐渐减弱、非金属性逐渐增强,故C错误;
D.O与S为同主族元素,同主族自上而下元素非金属性减弱,O比S的非金属性强,故D错误,
故选:B.
点评 本题考查元素周期律应用,比较基础,侧重对基础知识的巩固,注意掌握同主族、同周期元素性质递变规律.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
8.已知充分燃烧a g乙炔气体时生成1mol二氧化碳气体和0.5mol液态水,并放出热量b kJ,则表示乙炔燃烧热的热化学方程式正确的是( )
| A. | 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=-4b kJ/mol | |
| B. | C2H2(g)+$\frac{5}{2}$O2(g)═2CO2(g)+H2O(l)△H=-2b kJ/mol | |
| C. | 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=-2b kJ/mol | |
| D. | 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=-b kJ/mol |
20.取pH=2的盐酸和醋酸各100毫升,再分别加入0.65克锌粉,在相同条件下充分反应后,有关叙述正确的是( )
| A. | 刚开始醋酸与锌反应速率大 | |
| B. | 反应过程中盐酸和醋酸分别与锌反应的速率一样大 | |
| C. | 醋酸与锌反应放出的氢气多 | |
| D. | 锌分别与醋酸、盐酸反应产生的氢气一样多 |
17.今年春季,全国大范围的雾霾天气凸显出环境保护的重要性,为应对雾霾污染,改善空气质量,下列做法不合理的是( )
| A. | 加强汽车治理和垃圾处理场的建设和监管 | |
| B. | 实施“煤改气”、“煤改电”等清洁能源改造工程 | |
| C. | 研制新型高效可充电电池,发展纯电动汽车 | |
| D. | 加高工厂的烟囱,使烟尘和废气远离地表 |
15.设NA为阿伏加德罗常数,下列叙述正确的是( )
| A. | 常温常压下,22.4 L NO2中含有NA个分子 | |
| B. | 1 mol羟基中电子数为10 NA | |
| C. | R2+的质量数为A,中子数为N,则n g R该价态的氧化物中含质子数为$\frac{n}{A+16}$(A-N+8)NA | |
| D. | 在反应KIO3+6HI═KI+3I2+3H2O中,每生成3 mol I2转移的电子数为6 NA |
 ,请回答下列问题:
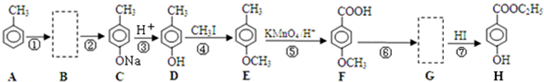
,请回答下列问题: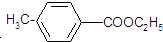 )是用于合成药物的中间体.请根据下列转化关系图回答有关问题:
)是用于合成药物的中间体.请根据下列转化关系图回答有关问题: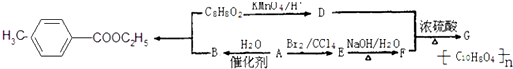
 .
.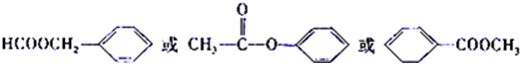 .
.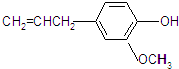 )是对甲基苯甲酸乙酯的同分异构体,下列物质与其能发生反应的是ACD(填序号).
)是对甲基苯甲酸乙酯的同分异构体,下列物质与其能发生反应的是ACD(填序号).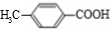 +CH3CH2OH$→_{△}^{浓硫酸}$
+CH3CH2OH$→_{△}^{浓硫酸}$
 .
. ,
,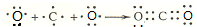 .
.
 .
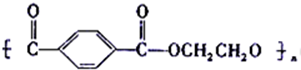
.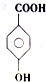 )在一定条件下发生聚合反应生成高分子化合物,写出该反应的化学方程式
)在一定条件下发生聚合反应生成高分子化合物,写出该反应的化学方程式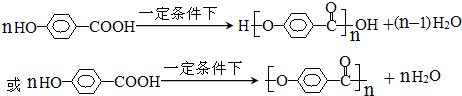 .
.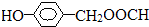 .
.