题目内容
12.下列叙述不正确的是( )| A. | Na+、Mg2+、Al3+的氧化性依次减弱 | B. | RbOH、KOH、Mg(OH)2的碱性依次减弱 | ||
| C. | H2S、H2O、HF的稳定性依次增强 | D. | H4SiO4、H2SO4、HClO4酸性依次增强 |
分析 A.根据元素周期律的递变规律判断对应元素金属性的强弱,元素的金属性越强,单质的还原性越强,阳离子的氧化性越弱;
B.根据元素周期律的递变规律判断对应元素金属性的强弱,元素的金属性越强,对应最高价氧化物的水化物的碱性越强;
C.根据元素周期律的递变规律判断对应元素非金属性的强弱,元素的非金属性越强,对应的氢化物越稳定;
D.根据元素周期律的递变规律判断对应元素非金属性的强弱,元素的非金属性越强,对应最高价氧化物的水化物的酸性越强.
解答 解:A.金属性:Al<Mg<Na,元素的金属性越强,单质的还原性越强,阳离子的氧化性越弱,Na+、Mg2+、Al3+的氧化性依次增强,故A错误;
B.金属性:Mg<K<Rb,元素的金属性越强,对应最高价氧化物的水化物的碱性越强,则碱性:Mg(OH)2<KOH<RbOH,故B正确;
C.非金属性:F>O>S,元素的非金属性越强,对应的氢化物越稳定,则稳定性:HF>H2O>H2S,故C正确;
D.非金属:Cl>S>Si,元素的非金属性越强,对应最高价氧化物的水化物的酸性越强,则酸性:HClO4>H2SO4>H4SiO4,故D正确;
故选A.
点评 本题考查元素性质的递变规律,题目难度不大,注意金属性和非金属性与对应单质、化合物的性质的联系.

练习册系列答案
相关题目
17.在室温下,同规格的铝片分别与下列物质混合,化学反应速率最大的是( )
| A. | 18mol/L的浓硫酸15mL L | B. | 0.2mol/L的盐酸12mL | ||
| C. | 0.15mol/L的硫酸溶液8mL | D. | 0.1mol/L的盐酸15m |
3.下列有关反应2NO+2CO$\frac{\underline{\;催化剂\;}}{△}$N2+CO2的叙述中,正确的是( )
| A. | 该反应是复分解反应 | B. | NO发生还原反应 | ||
| C. | CO是氧化剂 | D. | 反应物中O得电子 |
20.下列反应中,属于加成反应的是( )
| A. | 乙醇与金属钠反应 | B. | 苯和液溴反应生成溴苯 | ||
| C. | 乙烯和溴的四氯化碳溶液反应 | D. | 乙酸和乙醇反应生成乙酸乙酯 |
17.某实验小组用工业上废渣(主要成分Cu2S和Fe2O3)制取纯铜和绿矾(FeSO4•7H2O)产品,设计流程如下:

(1)在实验室中,欲用98%的浓硫酸(密度为1.84g•mL-1)配制500mL1.0mol•L-1的硫酸,需要的仪器除量筒、烧杯、玻璃棒外,还有胶头滴管、500mL容量瓶.
(2)该小组同学设计如下装置模拟废渣在过量氧气中焙烧,并验证废渣中含硫元素.
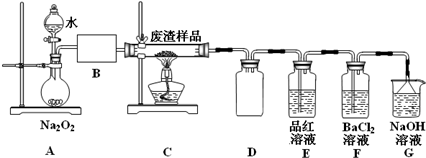
①装置A中反应的化学方程式为2Na2O2+2H2O=4NaOH+O2↑;为控制反应不过于激烈并产生平稳气流,采取的操作及现象是打开分液漏斗上口活塞,控制分液漏斗旋塞,使水匀速逐滴滴下;B处应连接盛有碱石灰的干燥管(或U形管)或浓硫酸的洗气瓶(填写试剂及仪器名称).
②E装置中加入品红溶液的目的是检验气体a中的SO2;当F装置中出现白色沉淀时,反应离子方程式为2SO2+O2+2H2O+2Ba2+=2BaSO4↓+4H+.
(3)下列操作中,不属于步骤⑤中进行的操作的是ad(填下列各项中序号).
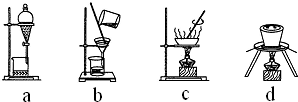
步骤⑥中由粗铜得到纯铜的方法为电解精炼(填写名称).
(4)为测定产品中绿矾的质量分数,称取30.000g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol•L-1酸性KMnO4溶液进行滴定,反应为:10FeSO4+8H2SO4+2KMnO4=2MnSO4+5Fe2(SO4)3+K2SO4+8H2O.实验所得数据如下表所示:
①第1组实验数据出现异常,造成这种异常的原因可能是ad(填代号).
a.酸式滴定管用蒸馏水洗净后未用标准液润洗
b.锥形瓶洗净后未干燥
c.滴定终点时俯视读数
d.滴定终点时仰视读数
②根据表中数据,计算所得产品中绿矾的质量分数为92.7%.

(1)在实验室中,欲用98%的浓硫酸(密度为1.84g•mL-1)配制500mL1.0mol•L-1的硫酸,需要的仪器除量筒、烧杯、玻璃棒外,还有胶头滴管、500mL容量瓶.
(2)该小组同学设计如下装置模拟废渣在过量氧气中焙烧,并验证废渣中含硫元素.

①装置A中反应的化学方程式为2Na2O2+2H2O=4NaOH+O2↑;为控制反应不过于激烈并产生平稳气流,采取的操作及现象是打开分液漏斗上口活塞,控制分液漏斗旋塞,使水匀速逐滴滴下;B处应连接盛有碱石灰的干燥管(或U形管)或浓硫酸的洗气瓶(填写试剂及仪器名称).
②E装置中加入品红溶液的目的是检验气体a中的SO2;当F装置中出现白色沉淀时,反应离子方程式为2SO2+O2+2H2O+2Ba2+=2BaSO4↓+4H+.
(3)下列操作中,不属于步骤⑤中进行的操作的是ad(填下列各项中序号).

步骤⑥中由粗铜得到纯铜的方法为电解精炼(填写名称).
(4)为测定产品中绿矾的质量分数,称取30.000g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol•L-1酸性KMnO4溶液进行滴定,反应为:10FeSO4+8H2SO4+2KMnO4=2MnSO4+5Fe2(SO4)3+K2SO4+8H2O.实验所得数据如下表所示:
| 滴定次数 | 1 | 2 | 3 | 4 |
| KMnO4溶液体积/mL | 20.90 | 20.02 | 19.98 | 20.00 |
a.酸式滴定管用蒸馏水洗净后未用标准液润洗
b.锥形瓶洗净后未干燥
c.滴定终点时俯视读数
d.滴定终点时仰视读数
②根据表中数据,计算所得产品中绿矾的质量分数为92.7%.
1.下列有关物质应用的说法错误的是( )
| A. | 用食醋清洗热水瓶中的水垢 | |
| B. | 工厂中常用的静电除尘装置是根据胶体带电这个性质而设计的 | |
| C. | 氢氧化铝可用于治疗胃酸过多 | |
| D. | 为了延长果实或花朵的成熟期,可用浸泡过高锰酸钾溶液的硅土吸收水果或花朵产生的乙烯 |
2.下列说法正确的是( )
| A. | 可用苯萃取四氯化碳中的碘 | |
| B. | 苯滴入溴水中,发生取代反应生成溴苯 | |
| C. | 可用石蕊溶液区分乙醇和乙酸两种物质 | |
| D. | 等物质的量的甲烷与氯气混合光照至充分反应,产物中最多的是四氯化碳 |
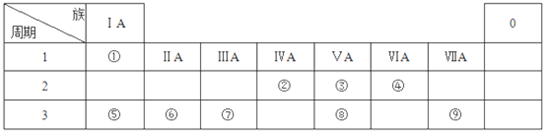
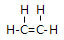 ;由④和⑥两种元素组成的化合物的电子式为
;由④和⑥两种元素组成的化合物的电子式为 ;元素⑨的原子结构示意图为
;元素⑨的原子结构示意图为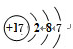 .
. 已知:SO2(g)+$\frac{1}{2}$O2(g)?SO3(g)△H=-98kJ•mol-1.
已知:SO2(g)+$\frac{1}{2}$O2(g)?SO3(g)△H=-98kJ•mol-1.