题目内容
18.以下表示物质通过一步反应的转化关系,下列说法正确的是( )X$\stackrel{O_{2}}{→}$酸性氧化物→还原性盐.
| A. | X可能是Si单质 | B. | X可能是含S元素的化合物 | ||
| C. | 酸性氧化物可能为CO2 | D. | 还原性盐可能为FeCl3 |
分析 A.Si和O2反应生成SiO2,SiO2和NaOH反应可生成Na2SiO3;
B.硫化氢和O2反应生成SO2;
C.CO2能形成碳酸盐;
D.FeCl3是非还原性盐.
解答 解:A.Si和O2反应生成SiO2,SiO2和NaOH反应可生成Na2SiO3,Na2SiO3不是还原性盐,故A错误;
B.硫化氢和O2反应生成SO2,SO2与氢氧化钠反应生成亚硫酸钠,亚硫酸钠是还原性盐,故B正确;
C.CO2能形成碳酸盐,碳酸盐是非还原性盐,故C错误;
D.FeCl3中铁是正三价,不能升高,是非还原性盐,故D错误.
故选B.
点评 本题综合考查元素化合物知识,侧重于物质的类别和性质的考查,题目难度不大,注意在学习中把握相关基础知识.

练习册系列答案
 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案
相关题目
8.有A、B、C、D四种金属,分别把它们加入到稀盐酸中,A、B、D反应后有气体放出,C无明显现象,再把A、D加入B盐溶液中,D表面有B析出,而A没有,则四种金属的活动性顺序是为( )
| A. | A>B>D>C | B. | B>D>A>C | C. | D>B>A>C | D. | D>A>B>C |
9.下列有关化学用语正确的是( )
| A. | 乙醇、乙二醇、丙三醇互为同系物,同系物之间不可能互为同分异构体 | |
| B. | 液化石油气和天然气的主要成分都是甲烷 | |
| C. | (CH3)2C=CHCH2CH3分子中的六个碳原子中至少有五个在同一个平面上 | |
| D. | 苯分子的比例模型: |
6.“神舟七号”宇宙飞船的能量部分来自太阳能电池,另外内部还配有高效的MCFC型燃料电池.该电池可同时供应电和水蒸气,所用燃料为氢气,电解质为熔融的碳酸钾.已知该电池的总反应为2H2+O2═2H2O,负极反应为H2+CO${\;}_{3}^{2-}$→CO2↑+H2O+2e-,则下列推断中,正确的是( )
| A. | 通氧气的电极为阳极,发生氧化反应 | |
| B. | 电池放电时,外电路电子由通氧气的正极流向通氢气的负极 | |
| C. | 正极的电极反应为:4OH-→O2↑+2H2O+2e- | |
| D. | 电池工作时,CO${\;}_{3}^{2-}$向负极移动 |
13.X、Y、Z、W是原子序数依次增大的四种短周期元素,甲是由其中的三种元素组成的化合物,0.lmol•L-1甲溶液的pH为13(25℃),Y元素最低负化合价的绝对值与其原子最外层电子数相等,下列说法正确的是( )
| A. | 原子半径:W>Z>Y>X | |
| B. | Y元素在周期表中的位置为第三周期第IVA族 | |
| C. | 与氢气化合时,Z比Y容易 | |
| D. | 甲中只含有离子键 |
3.有机物CH3CH2C(CH3)2CH(C2H5)CH3的准确命名是( )
| A. | 3,4-二甲基-4-己基戊烷 | B. | 3,3,4-三甲基己烷 | ||
| C. | 3,4,4-三甲基己烷 | D. | 2,3,3-三甲基己烷 |
7.下列过程中,共价键被破坏的是( )
| A. | 溴挥发 | B. | 氯气被木炭吸附 | C. | 食盐溶于水 | D. | 硫酸溶于水 |
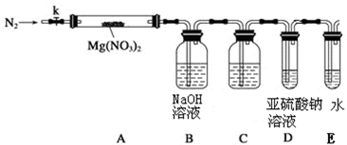 某学习小组以Mg(NO3)2为研究对象,拟通过实验初步探究硝酸盐热分解的规律.
某学习小组以Mg(NO3)2为研究对象,拟通过实验初步探究硝酸盐热分解的规律.