题目内容
4.常温下,下列盐的水溶液pH<7的是( )| A. | Na2CO3 | B. | Na2S | C. | FeCl3 | D. | NaCl |
分析 盐的水溶液pH值小于7,说明盐溶液是强酸弱碱盐,水解显酸性;或是弱酸的酸式盐溶液中当电离程度大于水解程度时;或是强酸的酸式盐溶液,能完全电离出氢离子时,据此分析.
解答 解:A、Na2CO3是强碱弱酸盐,水解显酸性,pH>7,故A错误;
B、Na2S是强碱弱酸盐,水解显酸性,pH>7,故B错误;
C、FeCl3溶液是强酸弱碱盐,溶液中铁离子水解显酸性,溶液pH<7,故C正确;
D、NaCl溶液是强酸强碱盐,溶液呈中性,溶液pH=7,故B错误;
故选C.
点评 本题考查了盐类水解的分析判断,溶液PH的变化,注意酸式盐的电离和水解程度比较,题目较简单.

练习册系列答案
相关题目
12.工业合成氨是人类科学技术上的一个重大突破,其反应过程为N2+3H2$?_{催化剂}^{高温高压}$2NH3;△H<0.若反应在恒容的容器中进行,下列由该反应的相关图象做出判断正确的是( )
| A | B | C | D |
 | 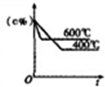 | 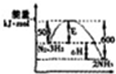 | 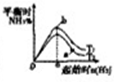 |
| P代表的是压强 | c%是氨气百分含量 | 1molN2和3molH2反应达平衡放出热量92kJ | 平衡常数:Kb>Ka |
| A. | A | B. | B | C. | C | D. | D |
9.X、Y、Z均为短周期元素,X、Y处于同一周期,X、Z的最低价离子分别为X2-和Z-,Y+和Z-具有相同的电子层结构,下列说法一定正确的是( )
| A. | 原子最外层电子数:Z>X>Y | B. | 单质沸点:X>Y>Z | ||
| C. | 离子半径:X2->Z->Y+ | D. | 原子序数:X>Z>Y |
16.实验室保存下列试剂的方法有错误的是( )
| A. | 新制氯气盛放在棕色试剂瓶中,存放于低温避光的地方 | |
| B. | 固体碘常盛放在棕色细口瓶中 | |
| C. | 液溴易挥发,盛放在用水液封的棕色试剂瓶中 | |
| D. | 金属钠易被氧化,少量金属钠应储存在煤油中 |

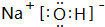
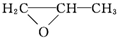 +H2O→
+H2O→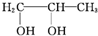 .
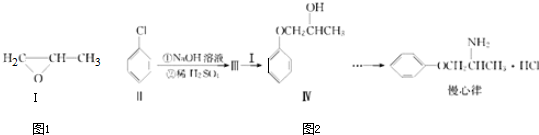
.
 .
.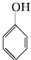 +3Br2→
+3Br2→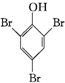 ↓+3HBr.
↓+3HBr.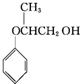 .
.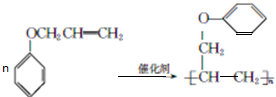 .
.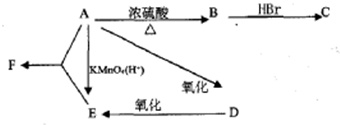 某有机物A,由C、H、O三种元素组成,在一定条件下由A可以转变为有机物B、C、D、E.转变关系如图所示.已知B是石油化工发展水平的标志.
某有机物A,由C、H、O三种元素组成,在一定条件下由A可以转变为有机物B、C、D、E.转变关系如图所示.已知B是石油化工发展水平的标志.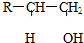 $→_{△}^{浓硫酸}$R-CH═CH2+H2O)
$→_{△}^{浓硫酸}$R-CH═CH2+H2O)