题目内容
6.同浓度的三种溶液:Na2SO4、MgSO4、Al2(SO4)3,其体积比为3:2:1,则SO${\;}_{4}^{2-}$浓度之比为3:2:3.×(判断对错)分析 根据溶液中不水解的离子的物质的量浓度=溶质的物质的量浓度×化学式中离子的个数,与溶液的体积无关,据此分析解答.
解答 解:假设三种溶液的浓度均为1mol/L,则Na2SO4、MgSO4、Al2(SO4)3溶液中SO${\;}_{4}^{2-}$浓度分别=1mol/L×1=1mol/L、1mol/L×1=1mol/L和1mol/L×3=3mol/L,即浓度之比为1:1:3,故答案为:×.
点评 本题考查物质的量浓度的计算与理解,题目难度不大,注意溶液中溶质离子的浓度与溶液体积无关,只取决于物质电离出的离子的数目多少与溶质的浓度.

练习册系列答案
 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案
相关题目
16.甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下转化关系:甲$\stackrel{丁}{→}$乙$?_{甲}^{丁}$丙.下列有关物质的推断不正确的是( )
| A. | 若甲为NH3,则丁可能是O2 | B. | 若甲为AlCl3,则丁可能是NaOH | ||
| C. | 若甲为NaOH溶液,则丁可能是CO2 | D. | 若甲为SiO2,则丁可能是C |
11.某离子的原子核里有n个质子,该离子的电子层排布与氩原子相同,它所带的电荷可能是( )
| A. | +(n-18) | B. | -n | C. | -(n+18) | D. | +(18-n) |
4.常温下,下列盐的水溶液pH<7的是( )
| A. | Na2CO3 | B. | Na2S | C. | FeCl3 | D. | NaCl |
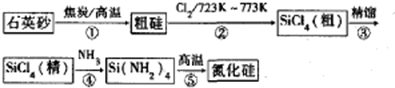
 .
.