题目内容
【题目】工业常用FeCl3溶液腐蚀附在绝缘板上的铜箔,制造印刷电路板。
(1)写出FeCl3溶液与金属铜反应的离子方程式____________________
(2)某小组采取下列步骤从使用过的腐蚀废液中回收铜,并重新获得FeCl3溶液。
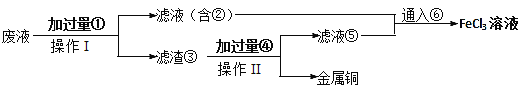
操作Ⅰ和Ⅱ的操作使用到的主要玻璃仪器有____,滤渣③含有的单质有______。通入气体⑥的化学式为______。
(3)若某腐蚀液中含1.5mol·L-1CuCl2、3.0mol·L-1FeCl2、1.0mol·L-1FeCl3,取200mL腐蚀液按上述步骤回收铜,为充分回收铜,加入①的质量最小为______。
【答案】Cu+2Fe3+=Cu2++2Fe2+ 漏斗、玻璃棒、烧杯 Cu,Fe Cl2 22.4g
【解析】
(1)铜与氯化铁反应生成氯化铜、氯化亚铁,据此分析书写反应的离子方程式;
(2)腐蚀废液中含有氯化亚铁、氯化铜,由工艺流程可知,滤渣③中含有金属铜,故应是废液与过量的Fe反应,滤液②中含有氯化亚铁,通入氯气可以得到氯化铁;滤渣③中含有金属铜、未反应的铁,加入盐酸,过滤,回收铜,滤液⑤中含有氯化亚铁,与滤液②合并,制备氯化铁,据此分析解答;
(3)由于氧化性Fe3+>Cu2+,故先发生反应:2Fe3++Fe=3Fe2+,然后再发生反应:Cu2++Fe=Fe2++Cu,结合方程式计算需要加入Fe的物质的量和质量。
(1)铜与氯化铁反应生成氯化铜、氯化亚铁,反应的离子方程式为:Cu+2Fe3+=Cu2++2Fe2+,故答案为:Cu+2Fe3+=Cu2++2Fe2+;
(2)反应后的废液中含有氯化亚铁、氯化铜,由工艺流程可知,滤渣③中含有金属铜,故应是废液与过量的Fe反应,滤液②中含有氯化亚铁,通入氯气可以得到氯化铁,滤渣③中含有金属铜、未反应的铁,加入盐酸,过滤,回收铜,滤液⑤中含有氯化亚铁,与滤液②合并,制备氯化铁。操作Ⅰ和Ⅱ都为过滤,用到的玻璃仪器有漏斗、玻璃棒、烧杯,滤渣③含有的单质有铜、铁,将氯化亚铁转化为氯化铁可以通入Cl2,故答案为:漏斗、玻璃棒、烧杯;铜、铁;Cl2;
(3)溶液中CuCl2为0.2L×1.5mol/L=0.3mol,FeCl2为0.2L×3mol/L=0.6mol,FeCl3为0.2L×1.0mol/L=0.2mol,为充分回收铜,加入的铁依次发生2个反应:2 Fe3++Fe=3 Fe2+和Cu2++Fe=Fe2++Cu,要将铜全部回收,加入Fe粉的质量应不少于(0.2mol×![]() +0.3mol)×56g/mol=22.4g,故答案为:22.4g。
+0.3mol)×56g/mol=22.4g,故答案为:22.4g。

【题目】某小组同学探究Cu和H2O2的反应。
(猜想预测)
猜想1:Cu与H2O2不发生反应;
猜想2:Cu与H2O2可能发生氧化还原反应,H2O2作氧化剂。
(实验探究)
实验ⅰ:向装有0.5 g Cu的烧杯中加入20 mL 30% H2O2溶液,一段时间内无明显现象,10 小时后,溶液中有少量蓝色浑浊,Cu片表面附着少量蓝色固体。
(1)通过该实验证明了猜想2成立,写出该反应的化学方程式:________。
(继续探究)
针对该反应速率较慢,小组同学查阅资料,设计并完成了下列实验。
资料:Cu2+ + 4NH3 [ Cu(NH3)4] 2+ ,[ Cu(NH3)4] 2+为深蓝色;Cu(OH)2可溶于氨水形成深蓝色溶液。
装置 | 序号 | 试剂a | 现象 |
| ⅱ | 20 mL 30% H2O与4 mL 5 mol/L H2SO4 混合液 | Cu表面很快生产少量气泡,溶液逐渐变蓝,产生较多气泡 |
ⅲ | 20 mL 30% H2O2与4 mL5 mol/L氨水混合液 | 溶液立即变为深蓝色,产生大量气泡,Cu表面有少量蓝色不溶物 |
(2)实验ⅱ中:溶液变蓝的原因是________(用化学用语解释);经检验产生的气体为氧气,产生氧气的原因是________。
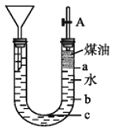
(3)对比实验ⅰ和ⅲ,为探究氨水对Cu的还原性或H2O2氧化性的影响,该同学利用如图装置继续实验。
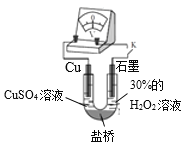
已知:电压大小反映了物质氧化还原性强弱的差异;物质氧化性与还原性强弱差异越大,电压越大。
a.K闭合时,电压为x。
b.向U型管右侧溶液中滴加氨水后,电压不变。
c.继续向U型管左侧溶液中滴加氨水后,电压增大了y。
该实验的结论:_________。利用该方法也可证明酸性增强可提高H2O2的氧化性,导致Cu溶解速率加快。
(4)对比实验ⅱ和ⅲ,实验ⅲ中产生氧气速率明显更快,可能的原因是_______。
(5)实验ⅲ有少量蓝色不溶物,小组同学加入少量NH4Cl可使其溶解,结合文字和化学用语解释不溶物溶解的原因:________。
(6)基于以上实验,影响Cu与H2O2反应速率的因素有________。
【题目】下表是几种弱酸常温下的电离平衡常数:
CH3COOH | H2CO3 | H2S | H3PO4 |
1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=9.1×10-8 K2=1.1×10-12 | K1=7.5×10-3 K2=6.2×10-8 K3=2.2×10-13 |
则下列说法中不正确的是( )
A. 碳酸的酸性强于氢硫酸
B. 多元弱酸的酸性主要由第一步电离决定
C. 常温下,加水稀释醋酸,![]() 增大
增大
D. 向弱酸溶液中加少量NaOH溶液,电离常数不变