��Ŀ����
����Ŀ��X��T��Y��ZΪ1��36��Ԫ�أ���ԭ������������������Ԫ�ص����ʻ�ṹ��Ϣ������������Ϣ�ش��������⣮
Ԫ�� | T | X | Y | Z |
���ʽṹ��Ϣ | ԭ�Ӻ���s������������p���������������ں�������Ԫ�أ����䵥���dz�������ȼ�� | ����Ϊ˫ԭ�ӷ��ӣ������к���3�Թ��õ��Ӷԣ������µ��������ȶ�������ԭ�ӽϻ��� | ��3����Ԫ�صļ������а뾶��С | ��4����Ԫ�أ�M���Ӳ�Ϊȫ����״̬�������ֻ��һ�����ӵ�ԭ�� |
��1��д��Ԫ��T�����ӽṹʾ��ͼ��д��Ԫ��X����̬�⻯��ĵ���ʽ��X�γɵĵ��ʷ��ӣ������Ҽ������м���д��ZԪ��ԭ�ӵ���Χ�����Ų�ʽ��Ԫ��Y��ԭ�Ӻ��������״��ͬ�ĵ����ƣ�
��2��Y����������������Һ��Ӧ�����ӷ���ʽ�� ��
��3��Ԫ��T���Ԫ����ȣ��ǽ����Խ�ǿ��������Ԫ�ط��ű�ʾ�������б�������֤����һ��ʵ�������������ĸ����
a�������·�������ɫ��T���ʵ���ɫ��
b��������T���⻯����ҷ�Ӧ������T�ĵ���
c������T�γɵĻ�������TԪ�س�����̬
d���Ƚ���Ԫ�صĵ�������������ʱ�õ��ӵ���Ŀ��
���𰸡�
��1�� ��
��![]() ��1��2��3d104s1��2
��1��2��3d104s1��2
��2��2Al+2OH��+2H2O=2AlO2��+3H2��
��3��F��bc
���������⣺��1��Ԫ��T������ΪO2�� �� O2�����ӽṹʾ��ͼΪ  ��Ԫ��X����̬�⻯��ΪNH3 �� ����ʽΪ
��Ԫ��X����̬�⻯��ΪNH3 �� ����ʽΪ ![]() ��N2�����д���N��N������1���Ҽ���2���м���ZΪCu����Χ�����Ų�ʽΪ3d104s1 �� YΪAl��������s��p�ܼ�������2�ֲ�ͬ��״�ĵ����ƣ����Դ��ǣ�
��N2�����д���N��N������1���Ҽ���2���м���ZΪCu����Χ�����Ų�ʽΪ3d104s1 �� YΪAl��������s��p�ܼ�������2�ֲ�ͬ��״�ĵ����ƣ����Դ��ǣ�  ��
�� ![]() ��1��2��3d104s1��2����2��Z����ΪAl��Y����������ˮ����ΪNaOH�����߷�Ӧ����ƫ����������������Ӧ�����ӷ���ʽΪ��2Al+2OH��+2H2O=2AlO2��+3H2����
��1��2��3d104s1��2����2��Z����ΪAl��Y����������ˮ����ΪNaOH�����߷�Ӧ����ƫ����������������Ӧ�����ӷ���ʽΪ��2Al+2OH��+2H2O=2AlO2��+3H2����
���Դ��ǣ�2Al+2OH��+2H2O=2AlO2��+3H2������3��Ԫ�������Ԫ����ȣ��ǽ����Խ�ǿ����FԪ�أ�
a��������ɫ�����������ʣ����ܱȽ�Ԫ�طǽ�����ǿ������a����
b��������T���⻯����ҷ�Ӧ������T�ĵ��ʣ�˵�����������Ը�ǿ������˵����Ԫ�طǽ�����ǿ����b��ȷ��
c������T�γɵĻ�������TԪ�س�����̬��˵��FԪ�ضԼ��ϵ���������ǿ�����Ԫ�طǽ����Ը�ǿ����c��ȷ��
d���ǽ�����ǿ�����õ������׳̶��йأ����õ�����Ŀ�����أ���d����
���Դ��ǣ�F��bc��

����Ŀ����NH3����ԭNxOy�������������������Ⱦ����֪����ӦI��4NH3��g��+6NO��g��5N2��g��+6H2O��l����H1
��ӦII��2NO��g��+O2��g��2NO2��g����H2 ����|��H1|=2|��H2|��
��ӦIII��4NH3��g��+6NO2��g��5N2��g��+3O2��g��+6H2O��l����H3
��ӦI�ͷ�ӦII�ڲ�ͬ�¶�ʱ��ƽ�ⳣ�������С��ϵ���±�
�¶�/K | ��ӦI | ��ӦII | ��֪�� |
298 | K1 | K2 | |
398 | K1�� | K2�� |
��1���ƲⷴӦIII����Ӧ������ȡ����ȡ���
��2����ͬ�����£���ӦI��2L�ܱ������ڣ�ѡ�ò�ͬ�Ĵ�������Ӧ����N2������ʱ��仯��ͼ1��ʾ���ټ���0��4������A���������£���Ӧ����v��NO��= ��
������˵����ȷ���� ��
A���÷�Ӧ�Ļ�ܴ�С˳���ǣ�Ea��A����Ea��B����Ea��C��
B������ѹǿ��ʹ��Ӧ���ʼӿ죬����Ϊ�����˻���Ӱٷ���
C����λʱ����H��O����N��H�����ѵ���Ŀ���ʱ��˵����Ӧ�Ѿ��ﵽƽ��
D�����ں��ݾ��ȵ��ܱ������з�����Ӧ����Kֵ����ʱ��˵����Ӧ�Ѿ��ﵽƽ��
��3��һ�������£���ӦII�ﵽƽ��ʱ��ϵ��n��NO����n��O2����n��NO2��=2��1��2����������������ʱ���ٳ���NO2���壬����NO2������������գ�NO2���ı仯���������������С�����䡱�����º�ѹ�������գ�NO2�������º����������գ�NO2�� ��
��4��һ���¶��£���ӦIII���ݻ��ɱ���ܱ������дﵽƽ�⣬��ʱ�ݻ�Ϊ3L��c��N2���뷴Ӧʱ��t�仯����X��ͼ2��ʾ������t1ʱ�̸ı�һ������������X��Ϊ����Y������Z���ٱ�Ϊ����Y�ı�������� �� ��Ϊ����Z�ı�������� �� 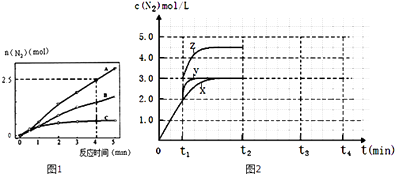
����t2�����¶ȣ�t3�ﵽƽ�⣬������ͼ�л�������X��t2��t4�� c��N2���ı仯���� ��