题目内容
9.有体积相同、pH相等的烧碱溶液和氨水,下列叙述中正确的是( )| A. | 两溶液中OH-离子浓度相同 | |
| B. | 用同浓度的盐酸中和时,消耗盐酸的体积相同 | |
| C. | 两溶液溶质物质的量浓度相同 | |
| D. | 加入等体积的水稀释后,它们的pH仍相等 |
分析 A.pH相等则氢氧根离子浓度相等;
B.用同浓度的盐酸中和时,消耗盐酸的体积与碱的物质的量成正比;
C.pH相等的NaOH和氨水,氨水浓度大于NaOH;
D.加水稀释促进弱电解质电离.
解答 解:A.pH相等的氨水和氢氧化钠,两种溶液中OH-浓度相同,故A正确;
B.用同浓度的盐酸中和时,消耗盐酸的体积与碱的物质的量成正比,pH相等、体积相等的氢氧化钠和氨水,氨水的物质的量大于氢氧化钠,所以氨水消耗的盐酸多,故B错误;
C.NaOH是强电解质,一水合氨是弱电解质,一水合氨存在电离平衡,pH相等的NaOH和氨水,氨水浓度大于NaOH,故C错误;
D.加水稀释促进弱电解质一水合氨电离,氢氧化钠完全电离,所以稀释相同的倍数后,氨水中氢氧根离子浓度大于氢氧化钠,故D错误;
故选A.
点评 本题考查了弱电解质的电离,根据弱电解质电离特点来分析解答,易错选项是B,注意:消耗酸的体积与碱的物质的量有关,与电解质强弱无关,为易错点.

练习册系列答案
相关题目
19.在某无色透明的碱性溶液中,能共存的离子组是( )
| A. | Na+、K+、SO42-、HCO3- | B. | Cu2+、K+、SO42-、NO3- | ||
| C. | Fe3+、K+、SO42-、Cl- | D. | Na+、K+、Cl-、NO3- |
20.在下列各组溶液中,离子一定能大量共存的是( )
| A. | 强碱性溶液中:Na+、K+、SO42-、AlO2- | |
| B. | 含有0.1 mol•L-1Fe3+的溶液中:K+、Mg2+、Cl-、SCN- | |
| C. | 某无色溶液中:NH4+、Fe2+、MnO4-、NO3- | |
| D. | 与铝反应生成H2的溶液中:Na+、K+、Cl-、SO42- |
17.要除去热水瓶中的水垢,可选用的试剂是( )
| A. | 食盐水 | B. | 烧碱溶液 | C. | 纯碱溶液 | D. | 稀醋酸 |
4.下列说法正确的是( )
| A. | 水俣病是因为长期食用富含汞的鱼和贝类而造成的慢性汞中毒 | |
| B. | 水俣病是长期食用含镉的污水灌溉的水稻造成的 | |
| C. | 日本的水俣病是有机汞引起的汞中毒 | |
| D. | 深海的生物对重金属离子的富集浓度大 |
14.同系物化学性质相似,由乙烯推测丙烯(CH3CH=CH2),下列说法不正确的是( )
| A. | 与溴水发生取代,反应产物的结构简式是CH3CBr2CH3 | |
| B. | 一定条件下能与水加成,产物是混合物 | |
| C. | 一定条件下能加聚合成  | |
| D. | 丙烯能使酸性高锰酸钾溶液褪色 |
1.相同物质的量的下列物质分别与等浓度的NaOH溶液反应,至体系中均无固体物质,消耗碱量最多的是( )
| A. | Al | B. | Al(OH)3 | C. | AlCl3 | D. | Al2O3 |
18.下列离子方程式正确的是( )
| A. | 水中加入钠:Na+2H2O═Na++2OH-+H2↑ | |
| B. | 碳酸氢钙溶液加入盐酸:CO32-+2H+═CO2↑+H2O | |
| C. | 氢氧化铜中加入盐酸:OH-+H+═H2O | |
| D. | 碳酸镁跟稀硫酸反应:MgCO3+2H+═Mg2++H2O+CO2↑ |
1.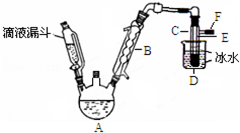 如图是实验室用乙醇与浓硫酸和溴化钠反应来制备溴乙烷的装置,反应需要加热,图中省去了加热装置.有关数据见表:
如图是实验室用乙醇与浓硫酸和溴化钠反应来制备溴乙烷的装置,反应需要加热,图中省去了加热装置.有关数据见表:
表.乙醇、溴乙烷、溴有关参数
(1)制备操作中,加入的浓硫酸必需进行稀释,其目的是abc(选填序号).
a.减少副产物烯和醚的生成 b.减少Br2的生成 c.减少HBr的挥发 d.水是反应的催化剂
(2)已知加热温度较低时NaBr与硫酸反应生成NaHSO4,写出加热时A中发生的主要反应的化学方程式CH3CH2OH+NaBr+H2SO4$\stackrel{△}{→}$NaHSO4+CH3CH2Br+H2O.
(3)仪器B的名称球形冷凝管,冷却水应从B的下(填“上”或“下”)口流进.
(4)反应生成的溴乙烷应在C中(填“A”或“C”中).
(5)若用浓的硫酸进行实验时,得到的溴乙烷呈棕黄色,最好选择下列b(选填序号)溶液来洗涤产品.
a.氢氧化钠 b.亚硫酸钠 c.碘化亚铁 d.碳酸氢钠
洗涤产品时所需要的玻璃仪器有分液漏斗、烧杯.
 如图是实验室用乙醇与浓硫酸和溴化钠反应来制备溴乙烷的装置,反应需要加热,图中省去了加热装置.有关数据见表:
如图是实验室用乙醇与浓硫酸和溴化钠反应来制备溴乙烷的装置,反应需要加热,图中省去了加热装置.有关数据见表:表.乙醇、溴乙烷、溴有关参数
| 乙醇 | 溴乙烷 | 溴 | |
| 状态 | 无色液体 | 无色液体 | 深红棕色液体 |
| 密度/g•cm-3 | 0.79 | 1.44 | 3.1 |
| 沸点/℃ | 78.5 | 38.4 | 59 |
a.减少副产物烯和醚的生成 b.减少Br2的生成 c.减少HBr的挥发 d.水是反应的催化剂
(2)已知加热温度较低时NaBr与硫酸反应生成NaHSO4,写出加热时A中发生的主要反应的化学方程式CH3CH2OH+NaBr+H2SO4$\stackrel{△}{→}$NaHSO4+CH3CH2Br+H2O.
(3)仪器B的名称球形冷凝管,冷却水应从B的下(填“上”或“下”)口流进.
(4)反应生成的溴乙烷应在C中(填“A”或“C”中).
(5)若用浓的硫酸进行实验时,得到的溴乙烷呈棕黄色,最好选择下列b(选填序号)溶液来洗涤产品.
a.氢氧化钠 b.亚硫酸钠 c.碘化亚铁 d.碳酸氢钠
洗涤产品时所需要的玻璃仪器有分液漏斗、烧杯.