题目内容
8.在一定条件下的密闭容器中,一定能说明反应A(g)+3B(g)?2C(g)+2D(g)达到平衡状态的是( )| A. | 反应体系的总压恒定 | B. | A、B的浓度相等 | ||
| C. | c(A):c(B)=1:3 | D. | 2v(B)正=3v(C)逆 |
分析 根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:A、两边的气体计量数相等,所以反应体系的总压一直恒定,故A错误;
B、A、B的浓度可能相等,也可能不等,与各物质的初始浓度及转化率有关,故B错误;
C、当体系达平衡状态时,A和B的浓度之比可能为1:3,也可能不是1:3,与各物质的初始浓度及转化率有关,故C错误;
D、2v(B)正=3v(C)正=3v(C)逆,故D正确;
故选D.
点评 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案
相关题目
3.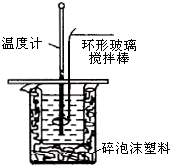 利用如图装置测定中和热的实验步骤如下:
利用如图装置测定中和热的实验步骤如下:
①量取50mL 0.25mol/L硫酸倒入小烧杯中,测量温度;
②量取50mL 0.55mol/L NaOH溶液,测量温度;
③将NaOH溶液倒入小烧杯中,混合均匀后测量混合液温度.
请回答:
(1)NaOH溶液稍过量的原因确保硫酸被完全中和.
(2)加入NaOH溶液的正确操作是B(填字母).
A.沿玻璃棒缓慢加入 B.一次迅速加入 C.分三次加入
(3)使硫酸与NaOH溶液混合均匀的正确操作是用环形玻璃棒轻轻搅动.
(4)设溶液的密度均为1g/cm3,中和后溶液的比热容c=4.18J/(g•℃),请根据实验数据写出该反应的热化学方程式H2SO4(aq)+2NaOH(aq)Na2SO4(aq)+2H2O(l);△H=-113.7kJ•mol-1.
(5)若将含0.5mol H2SO4的浓硫酸与含1mol NaOH的溶液混合,放出的热量大于(填“小于”、“等于”或“大于”)57.3kJ,原因是浓硫酸溶于水放出热量.
 利用如图装置测定中和热的实验步骤如下:
利用如图装置测定中和热的实验步骤如下:①量取50mL 0.25mol/L硫酸倒入小烧杯中,测量温度;
②量取50mL 0.55mol/L NaOH溶液,测量温度;
③将NaOH溶液倒入小烧杯中,混合均匀后测量混合液温度.
请回答:
(1)NaOH溶液稍过量的原因确保硫酸被完全中和.
(2)加入NaOH溶液的正确操作是B(填字母).
A.沿玻璃棒缓慢加入 B.一次迅速加入 C.分三次加入
(3)使硫酸与NaOH溶液混合均匀的正确操作是用环形玻璃棒轻轻搅动.
(4)设溶液的密度均为1g/cm3,中和后溶液的比热容c=4.18J/(g•℃),请根据实验数据写出该反应的热化学方程式H2SO4(aq)+2NaOH(aq)Na2SO4(aq)+2H2O(l);△H=-113.7kJ•mol-1.
| 温度 实验次数 | 起始温度t1/℃ | 终止温度 t2/℃ | 温度差平均值(t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 25.0 | 25.2 | 25.1 | 28.5 | 3.4 |
| 2 | 24.9 | 25.1 | 25.0 | 28.3 | 3.3 |
| 3 | 25.6 | 25.4 | 25.5 | 29.0 | 3.5 |
4.下列有关物质性质与应用对应关系正确的是( )
| A. | 炭具有还原性,一定条件下能将二氧化硅还原为硅 | |
| B. | 二氧化硫具有还原性,能用于漂白纸浆 | |
| C. | 碳酸钠能和酸反应,常用于治疗胃酸过多 | |
| D. | 氧化铝熔点很高,用其制造的坩埚可用于熔融烧碱 |
3.被称为“智慧元素”--碘的单质及其化合物应用十分广泛,碘化钠常用于医疗和照相业等.某实验小组模拟其工业制备工艺流程如图1:

请回答下列问题:
(1)操作A包括加热浓缩、冷却结晶、过滤;用冰水洗涤的目的是洗涤除去表面可溶性杂质,同时尽量减少NaI的溶解损失;反应②的离子方程式为2Fe+IO3-+3H2O═2Fe(OH)3+I-.
(2)某同学推测得到的成品除含有NaI外,还可能有NaIO3和NaOH,并设计如下方案进行检验,实验结果表明其推测正确.
已知:IO3-+5I-+6H+=3I2+3H2O2;NaIO3水溶液呈中性.
限选试剂:1mol•L-1H2SO4溶液、2mol•L-1HNO3溶液、淀粉溶液、酚酞试液、石蕊试液、蒸馏水.其它仪器和用品自选.
(3)如图2装置Ⅰ为一种可充电电池的示意图,其中的离子交换膜只允许Na+通过,该电池充、放电的化学方程式为Na2S4+3NaI$?_{放电}^{充电}$2Na2S2+NaI3,装置Ⅱ为电解池的示意图.当闭合开关S时,电极X附近溶液先变红.此时,电极B上发生反应的电极反应式为NaI3+2Na++2e-=3NaI.电极Y上发生氧化(填“氧化”、“还原”)反应.装置Ⅱ溶液的体积为100mL,电解结束后若X极生成1.12L(已换算成标准状况)气体,则此时溶液的pH=14(假设溶液体积没有变化).

请回答下列问题:
(1)操作A包括加热浓缩、冷却结晶、过滤;用冰水洗涤的目的是洗涤除去表面可溶性杂质,同时尽量减少NaI的溶解损失;反应②的离子方程式为2Fe+IO3-+3H2O═2Fe(OH)3+I-.
(2)某同学推测得到的成品除含有NaI外,还可能有NaIO3和NaOH,并设计如下方案进行检验,实验结果表明其推测正确.
已知:IO3-+5I-+6H+=3I2+3H2O2;NaIO3水溶液呈中性.
限选试剂:1mol•L-1H2SO4溶液、2mol•L-1HNO3溶液、淀粉溶液、酚酞试液、石蕊试液、蒸馏水.其它仪器和用品自选.
| 实验方案 | 实验现象 | 结论 |
| 将白色晶体溶于水,并滴2滴淀粉溶液 | 得到无色溶液 | |
| 取少量溶液于试管A中,加入足量的1mol•L-1H2SO4 | 溶液呈蓝色 | 溶液中含IO3- |
| 另取少量溶液于试管B中,滴入几滴酚酞溶液 | 溶液变红 | 溶液中含大量OH- |
13.下表中的数据是破坏或生成1mol物质中的化学键所消耗或吸收的能量(单位:kJ):
根据上述数据回答:
(1)下列氢化物中最稳定的是A(填序号).
A.HCl B.HRr C.HI
(2)有表中数据推知反应I2+H2=2HI释放能量(填“吸收”或“释放”).
(3)相同条件下,X2(X代表Cl、Rr、I)分别与氢气反应,当消耗等物质的量的氢气时,放出或吸收的能量最多的是Cl2(填化合物的方程式).
(4)若无上表中的数据,你能正确回答出问题(3)吗?
答:能(填“能”或“不能”);简述你的理由同主族元素按I、Br、Cl的顺序原子得电子能力渐强,生成的HX越趋稳定,相应释放出能量越多.
根据上述数据回答:
| 物质 | Cl2 | Rr2 | I2 | HCl | HBr | HI | H2 |
| 能量(kJ) | 243 | 193 | 151 | 432 | 366 | 298 | 436 |
A.HCl B.HRr C.HI
(2)有表中数据推知反应I2+H2=2HI释放能量(填“吸收”或“释放”).
(3)相同条件下,X2(X代表Cl、Rr、I)分别与氢气反应,当消耗等物质的量的氢气时,放出或吸收的能量最多的是Cl2(填化合物的方程式).
(4)若无上表中的数据,你能正确回答出问题(3)吗?
答:能(填“能”或“不能”);简述你的理由同主族元素按I、Br、Cl的顺序原子得电子能力渐强,生成的HX越趋稳定,相应释放出能量越多.
20.某元素二价阴离子核外有18个电子,质量数为32,该元素氢化物1mol含中子数( )
| A. | 12 mol | B. | 14 mol | C. | 16 mol | D. | 18 mol |
18. 如表列出了部分元素在周期表中的位置,请用具体的元素完成下列填空.
如表列出了部分元素在周期表中的位置,请用具体的元素完成下列填空.
(1)上述元素的原子中,得电子能力最强的是氟(填元素名称).
(2)E元素与Q元素两者核电荷数之差是18.
(3)G对应离子的半径>Z对应离子的半径(填“<”或“>”).
(4)写出H与Z的最高价氧化物的水化物溶液反应的离子方程式:2Al+2OH-+2H2O═2AlO2-+2H2↑.
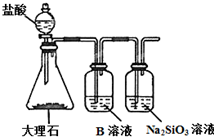
(5)为比较元素X和W的非金属性强弱,用如图所示装置进行实验(夹持仪器已略去,装置气密性良好).溶液B的作用是除去CO2中的HCl,能说明X和W非金属性强弱的离子方程式是CO2+SiO32-+H2O═CO32-+H2SiO3↓.
 如表列出了部分元素在周期表中的位置,请用具体的元素完成下列填空.
如表列出了部分元素在周期表中的位置,请用具体的元素完成下列填空.| 族 周期 | ⅠA | 0 | ||||||||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||||||||
| 2 | X | Y | G | |||||||||||
| 3 | Z | … | H | W | E | |||||||||
| 4 | … | Q | ||||||||||||
(2)E元素与Q元素两者核电荷数之差是18.
(3)G对应离子的半径>Z对应离子的半径(填“<”或“>”).
(4)写出H与Z的最高价氧化物的水化物溶液反应的离子方程式:2Al+2OH-+2H2O═2AlO2-+2H2↑.
(5)为比较元素X和W的非金属性强弱,用如图所示装置进行实验(夹持仪器已略去,装置气密性良好).溶液B的作用是除去CO2中的HCl,能说明X和W非金属性强弱的离子方程式是CO2+SiO32-+H2O═CO32-+H2SiO3↓.
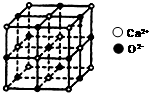 (1)AlN的晶体结构与单晶硅相似,在AlN晶体中,每个Al原子与4个N原子相连,与N元素同主族的元素As位于元素周期表的第四周期,其基态原子的核外电子排布式为1s22s22p63s23p63d104s24p3.
(1)AlN的晶体结构与单晶硅相似,在AlN晶体中,每个Al原子与4个N原子相连,与N元素同主族的元素As位于元素周期表的第四周期,其基态原子的核外电子排布式为1s22s22p63s23p63d104s24p3.