题目内容
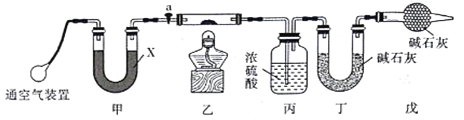
【题目】已知木炭在一定条件下与浓硝酸反应生成两种+4价的氧化物,为了探究一氧化氮(NO)能否与过氧化钠反应,以及反应后的产物中是否有亚硝酸钠(NaNO2),某小组同学设计了如图所示装置(夹持仪器和连接用的胶管已经省略)。
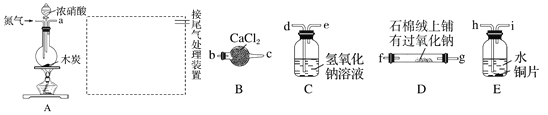
(1)为了完成该实验,虚线框内还需要连接B~E四套装置,按气流方向连接的顺序为:
a→( )( )→( )( )→( )( )→ ( )( )(填仪器接口的字母编号)。连接好仪器,检查气密性,装入药品后,要通入一段时间的氮气,再滴加浓硝酸,点燃酒精灯,通入氮气的主要目的是 。
(2)装置E中观察到的主要实验现象有 。
(3)装置C的作用是 。
(4)某同学经查阅资料后发现亚硝酸是弱酸,性质不稳定,室温下易分解生成一氧化氮。装置D中充分反应后,设计实验证明D中是否有亚硝酸钠生成: 。(写出检验步骤及现象)。
(5)亚硝酸钠在酸性条件下可将I-氧化为I2,同时生成NO,该反应常用于亚硝酸钠含量的测定,请写出该反应的离子方程式: 。
【答案】(1)hi→de→bc→fg(或gf)排除装置中的空气,防止NO被空气中氧气氧化为NO2;
(2)溶液由无色变成蓝色,有无色气体逸出
(3)吸收CO2,除去NO中的NO2
(4)取少量D中的固体于试管中,加入稀硫酸,若溶液中有气泡产生且在试管液面上方变成红棕色气体,则D中有亚硝酸钠生成。
(5)2NO2-+2I-+4H+=2NO↑+I2+2H2O
【解析】木炭与浓硝酸反应在加热条件下生成NO2和CO2,装置E是将NO2溶于水转化成NO和HNO3,稀硝酸和铜反应又生成NO;装置C的作用是吸收CO2,除去NO中的NO2;装置B的作用起干燥作用;亚硝酸不稳定,易分解生成NO,所以检验亚硝酸钠,是将其变成HNO2,检验其产物NO就行了;