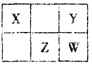题目内容
【题目】A、B、C、D均为中学化学中常见的单质或化合物,它们之间的关系如图a所示(部分产物已略去)。
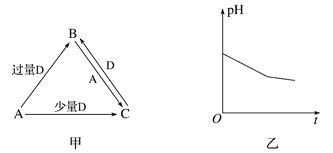
(1)若A为非金属单质,D是空气的主要成分之一,请写出B的电子式______________。
(2)若A为金属单质,D是某强酸的稀溶液,则反应C+D→B的离子方程式为_____________________。
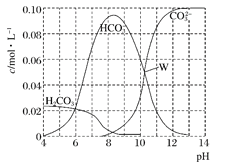
(3)若A为强碱,D为气态氧化物。B的水溶液露置于空气中一段时间,其pH变化如图b所示,则其pH变化的原因是____________(用离子方程式表示)。
【答案】(1)![]() (2分)
(2分)
(2)3Fe2++4H++NO3-=3Fe3++NO↑+2H2O(2分)
(3)2HSO3-+O2 = 2H++2SO42-(2分)
【解析】试题分析:(1)若A为非金属单质,可以是碳单质,与D氧气反应生成一氧化碳和二氧化碳,则B为二氧化碳,其电子式为:![]() ;
;
(2)若A为金属单质,D是某强酸的稀溶液,A和D反应时,A的量不同生成物不同,则A是变价金属,且A是常见金属,则A为铁,B是铁盐,C是亚铁盐,D为稀硝酸,则反应C+D→B的离子方程式为3Fe2+ + 4H+ + NO3- = 3Fe3+ + NO↑ + 2H2O;
(3)若A为强碱,D为气态氧化物,判断D为SO2,B为亚硫酸氢盐,常温时,将B的水溶液露置于 空气中,图2中pH变化判断为酸性增强,pH减小;所以是HSO3-被氧气氧化的结果,反应为2HSO3- + O2 = 2H+ + 2SO42-;

练习册系列答案
相关题目