题目内容
16.2mol O3和3mol O2的质量比为1:1;分子数之比为2:3;含有氧原子的数目之比为1:1;在相同条件下气体的体积比为2:3.同温同容下二者的压强比为2:3.分析 2mol O3和3mol O2,根据m=nM计算O2和O3的质量,进而计算二者质量之比;
O3中O原子的物质的量为O3的3倍,O2中O原子的物质的量为O2的2倍,原子数目之比等于物质的量之比;
同温同压下体积之比等于物质的量之比;同温同容下,压强之比等于物质的量之比.
解答 解:2molO3的质量为2mol×48g/mol=96g,3molO2的质量为3mol×32g/mol=96g,故二者质量之比为96g:96g=1:1;
分子数之比等于物质的量之比等于2:3;
O3中O原子的物质的量为O3的3倍,2molO3含有O原子物质的量为6mol,O3中O原子的物质的量为O3的3倍,2molO3含有O原子物质的量为6mol,故二者含有O原子数目之比为1:1;
同温同压下体积之比等于物质的量之比,故2mol O3和3mol O2的体积之比为2:3,
同温同容下,压强之比等于物质的量之比为2:3;
故答案为:1:1;2:3;1:1;2:3;2:3.
点评 本题考查常用化学计量的有关计算、物质中原子数目的计算等,比较基础,注意根据化学式确定原子数目与物质的物质的量关系.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
7.某学生用托盘天平称量食盐,将食盐放在右盘,砝码放在左盘,称得食盐的质量为15.5g(1g以下用游码).该学生所称量的食盐的实际质量是( )
| A. | 15.5 g | B. | 15.0 g | C. | 14.5 g | D. | 16.0 g |
4.除去溶液中溶解的杂质,下列做法中不正确的是(括号内的物质为杂质)( )
| A. | NaCl溶液(Na2SO4)加入适量Ba(NO3)2溶液后,过滤 | |
| B. | NaNO3溶液(NaCl)加入适量AgNO3溶液后,过滤 | |
| C. | NaCl溶液(CaCl2)加入适量Na2CO3溶液后,过滤 | |
| D. | NaCl溶液(碘I2)加入四氯化碳后,分液 |
11.在相同条件下,两种气体的物质的量相同,下列说法一定正确的是( )
| A. | 体积均为22.4 L | B. | 具有相同的体积 | ||
| C. | 具有相同的质量 | D. | 具有相同的原子数目 |
1.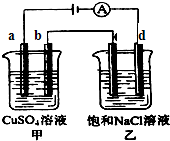 如图两个电解槽中,a、b、c、d均为石墨电极.若电解过程中共有0.02mol电子通过,下列叙述中正确的是( )
如图两个电解槽中,a、b、c、d均为石墨电极.若电解过程中共有0.02mol电子通过,下列叙述中正确的是( )
 如图两个电解槽中,a、b、c、d均为石墨电极.若电解过程中共有0.02mol电子通过,下列叙述中正确的是( )
如图两个电解槽中,a、b、c、d均为石墨电极.若电解过程中共有0.02mol电子通过,下列叙述中正确的是( )| A. | 甲烧杯中a极上最多可析出铜0.64g | |
| B. | 甲烧杯中b极上电极反应式4OH--4e-═2H2O+O2↑ | |
| C. | 乙烧杯中滴入酚酞试液,d极附近先变红 | |
| D. | 烧杯中c极上电极反应式为4H++4e-═2H2↑ |
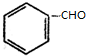 +H2(足量):
+H2(足量):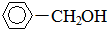 .
.