题目内容
15.下列物质性质的递变关系正确的是( )| A. | 酸性强弱:HClO3>H2SO3>H3PO4 | B. | 碱性:NaOH>KOH>Ca(OH)2>Mg(OH)2 | ||
| C. | 稳定性HCl>H2S>PH3 | D. | 氧化性Na+>Mg2+>Al3+ |
分析 A.元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强;
B.元素的金属性越强,对应的最高价氧化物的水化物的碱性越强;
C.元素的非金属性越强,对应的氢化物的稳定性越强;
D.金属单质的还原性越强,对应的离子的氧化性越弱.
解答 解:A.非金属性Cl>S>P,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,应为HClO4>H2SO4>H3PO4,否则不能比较酸性强弱,故A错误;
B.金属性K>Ca>Na>Mg,元素的金属性越强,对应的最高价氧化物的水化物的碱性越强,因Ca(OH)2溶解度较小,则碱性KOH>NaOH>Ca(OH)2>Mg(OH)2,故B错误;
C.非金属性Cl>S>P,元素的非金属性越强,对应的氢化物的稳定性越强,故C正确;
D.金属单质的还原性Na>Mg>Al,氧化性Na+<Mg2+<Al3+,故D错误.
故选C.
点评 本题考查元素周期律知识,为高考高频考点,侧重于学生的分析能力的考查,注意把握元素的性质与对应单质、化合物的性质的关系以及比较角度,难度不大.

练习册系列答案
相关题目
3.除去Na2CO3 固体中混有少量NaHCO3的最佳方法是( )
| A. | 加入适量盐酸 | B. | 加入NaOH溶液 | ||
| C. | 置于坩埚中加热 | D. | 配成溶液后通入CO2 |
4.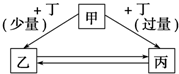 甲、乙、丙、丁均为中学化学中常见的物质,它们之间存在如图所示的转化关系(部分产物略去),甲不可能是( )
甲、乙、丙、丁均为中学化学中常见的物质,它们之间存在如图所示的转化关系(部分产物略去),甲不可能是( )
 甲、乙、丙、丁均为中学化学中常见的物质,它们之间存在如图所示的转化关系(部分产物略去),甲不可能是( )
甲、乙、丙、丁均为中学化学中常见的物质,它们之间存在如图所示的转化关系(部分产物略去),甲不可能是( )| A. | NaOH溶液 | B. | Fe | C. | Al2O3 | D. | C |
3. 实验室用乙酸和正丁醇制备乙酸正丁酯.有关物质的相关数据如下表.
实验室用乙酸和正丁醇制备乙酸正丁酯.有关物质的相关数据如下表.
(一)乙酸正丁酯的制备
①在干燥的50mL圆底烧瓶中,加入13.5mL正丁醇和7.2mL冰醋酸,再加入3~4滴浓硫酸,摇匀,投入1~2粒沸石.然后安装分水器(作用:实验过程中不断分离除去反应生成的水)、温度计及回流冷凝管,加热冷凝回流反应
(二)产品的精制
②将分水器分出的酯层和反应液一起倒入分液漏斗中,用10mL的水洗涤.有机层继续用10mL 10% Na2CO3洗涤至中性,再用10mL的水洗涤,最后将有机层转移至锥形瓶中,再用无水硫酸镁干燥.
③将干燥后的乙酸正丁酯滤入50mL烧瓶中,常压蒸馏,收集125~127℃的馏分,得11.6g乙酸正丁酯
请回答有关问题.
(1)冷水应该从冷凝管a(填a或b)管口通入.
(2)步骤①中不断从分水器下部分出生成的水的目的是使用分水器分离出水,使平衡正向移动,提高反应产率,步骤①中判断反应终点的依据是分水器中的水层量不再增加.
(3)产品的精制过程步骤②中,第一次水洗的目的是除去乙酸及少量的正丁醇,用饱和Na2CO3溶液洗涤有机层,该步操作的目的是除去产品中含有的乙酸等杂质.
(4)下列关于分液漏斗的使用叙述正确的是D
A.分液漏斗使用前必须要检漏,只要分液漏斗的旋塞芯处不漏水即可使用
B.装液时,分液漏斗中液体的总体积不得超过其容积的$\frac{2}{3}$
C.萃取振荡操作应如图所示
D.放出液体时,需将玻璃塞打开或使塞上的凹槽对准漏斗口上的小孔
(5)步骤③的常压蒸馏,需收集126℃的馏分,沸点大于140℃的有机化合物的蒸馏,一般不用上述冷凝管而用空气冷凝管,可能原因是防止因温差过大,冷凝管炸裂
(6)该实验过程中,生成乙酸正丁酯(式量116)的产率是80%.
 实验室用乙酸和正丁醇制备乙酸正丁酯.有关物质的相关数据如下表.
实验室用乙酸和正丁醇制备乙酸正丁酯.有关物质的相关数据如下表.| 化合物 | 相对分子质量 | 密度/g•cm-3 | 沸点/℃ | 溶解度/100g水 |
| 正丁醇 | 74 | 0.80 | 118.0 | 9 |
| 冰醋酸 | 60 | 1.045 | 118.1 | 互溶 |
| 乙酸正丁酯 | 116 | 0.882 | 126.1 | 0.7 |
①在干燥的50mL圆底烧瓶中,加入13.5mL正丁醇和7.2mL冰醋酸,再加入3~4滴浓硫酸,摇匀,投入1~2粒沸石.然后安装分水器(作用:实验过程中不断分离除去反应生成的水)、温度计及回流冷凝管,加热冷凝回流反应
(二)产品的精制
②将分水器分出的酯层和反应液一起倒入分液漏斗中,用10mL的水洗涤.有机层继续用10mL 10% Na2CO3洗涤至中性,再用10mL的水洗涤,最后将有机层转移至锥形瓶中,再用无水硫酸镁干燥.
③将干燥后的乙酸正丁酯滤入50mL烧瓶中,常压蒸馏,收集125~127℃的馏分,得11.6g乙酸正丁酯
请回答有关问题.
(1)冷水应该从冷凝管a(填a或b)管口通入.
(2)步骤①中不断从分水器下部分出生成的水的目的是使用分水器分离出水,使平衡正向移动,提高反应产率,步骤①中判断反应终点的依据是分水器中的水层量不再增加.
(3)产品的精制过程步骤②中,第一次水洗的目的是除去乙酸及少量的正丁醇,用饱和Na2CO3溶液洗涤有机层,该步操作的目的是除去产品中含有的乙酸等杂质.
(4)下列关于分液漏斗的使用叙述正确的是D
A.分液漏斗使用前必须要检漏,只要分液漏斗的旋塞芯处不漏水即可使用
B.装液时,分液漏斗中液体的总体积不得超过其容积的$\frac{2}{3}$
C.萃取振荡操作应如图所示
D.放出液体时,需将玻璃塞打开或使塞上的凹槽对准漏斗口上的小孔
(5)步骤③的常压蒸馏,需收集126℃的馏分,沸点大于140℃的有机化合物的蒸馏,一般不用上述冷凝管而用空气冷凝管,可能原因是防止因温差过大,冷凝管炸裂
(6)该实验过程中,生成乙酸正丁酯(式量116)的产率是80%.
20.下列粒子半径大小的比较中正确的是( )
| A. | r(S2-)>r(O2-)>r(F-) | B. | r(Al)>r(Mg)>r(Na) | C. | r(Na+)>r(O2-)>r(F-) | D. | r(Na)>r(Na+)>r(Cl-) |
5.有关金属晶体的下列说法正确的是( )
| A. | 金属晶体能导电,所以离子晶体也能导电 | |
| B. | 六方最密堆积和面心立方最密堆积中由于配位数都是12,所以所得晶胞的形式相同 | |
| C. | 金属晶体中金属原子的堆积模式有4种 | |
| D. | 金属晶体的电子气理论不能解释金属的延展性,但可以解释金属的导电性和熔点高低 |

 如图是常见原电池装置,电流表G发生偏转:
如图是常见原电池装置,电流表G发生偏转: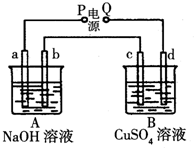 按如图装置实验,A、B两烧杯分别盛放200g 10%NaOH和足量CuSO4溶液.通电一段时间后,c极上有Cu析出;又测得A杯中溶液的质量减少4.5g(不考虑水的蒸发).a、b、c为石墨电极,d为铜电极.
按如图装置实验,A、B两烧杯分别盛放200g 10%NaOH和足量CuSO4溶液.通电一段时间后,c极上有Cu析出;又测得A杯中溶液的质量减少4.5g(不考虑水的蒸发).a、b、c为石墨电极,d为铜电极.